|
百蓁生物DeepImmu新抗原發(fā)現(xiàn)平臺通過建立高通量高靈敏度樣品前處理及質(zhì)譜檢測技術(shù)流程,整合DeepNovo數(shù)據(jù)分析和免疫原性預(yù)測新算法可實現(xiàn)一周時間內(nèi)“多.快.好.準(zhǔn)”的新生抗原發(fā)現(xiàn)
|
||||||||||||||||||
| [發(fā)表評論] [本類其他服務(wù)] [本類其他服務(wù)商] | ||||||||||||||||||
| 服務(wù)商: 百蓁生物技術(shù)(武漢)有限公司 | 查看該公司所有服務(wù) >> |
利用 T 細(xì)胞靶向和殺死特定的癌細(xì)胞類型(即免疫療法)已成為新型癌癥療法的前沿, CAR-T 療法已在多種適應(yīng)癥中顯示出顯著的療效,但在靶向?qū)嶓w瘤、功能持久性、腫瘤逃逸和避免復(fù)發(fā)方面仍需改進(jìn)。越來越多的研究強調(diào)了新抗原與T 細(xì)胞識別癌細(xì)胞之間的關(guān)系。針對新抗原開發(fā)的疫苗現(xiàn)在正用于各種實體瘤的臨床試驗。
新抗原(Neoantigen)是一類由腫瘤細(xì)胞突變而產(chǎn)生的腫瘤特異性抗原。它主要在腫瘤細(xì)胞中表達(dá)新抗原,也可以通過病毒感染、可變剪接和基因重排產(chǎn)生。它們是T 細(xì)胞識別癌細(xì)胞的理想靶標(biāo),可以激發(fā)強烈的抗腫瘤免疫反應(yīng)。
百蓁生物DeepImmu新抗原發(fā)現(xiàn)平臺通過建立高通量高靈敏度樣品前處理及質(zhì)譜檢測技術(shù)流程,整合DeepNovo數(shù)據(jù)分析和免疫原性預(yù)測新算法可實現(xiàn)一周時間內(nèi)“多.快.好.準(zhǔn)”的新生抗原發(fā)現(xiàn),為后續(xù)免疫治療研發(fā)提供強有力支持。
多 :鑒定深度超越30000+免疫多肽,突破10mg組織樣品極限(5000+多肽)
快 :一周實現(xiàn)從樣本處理到新抗原預(yù)測報告
好:實驗重現(xiàn)性好,免疫肽富集有效性高,譜圖質(zhì)量好,全流程質(zhì)控
準(zhǔn):AI賦能的新抗原免疫原性預(yù)測,驅(qū)動高效的驗證平臺,篩選新抗原更準(zhǔn)確。
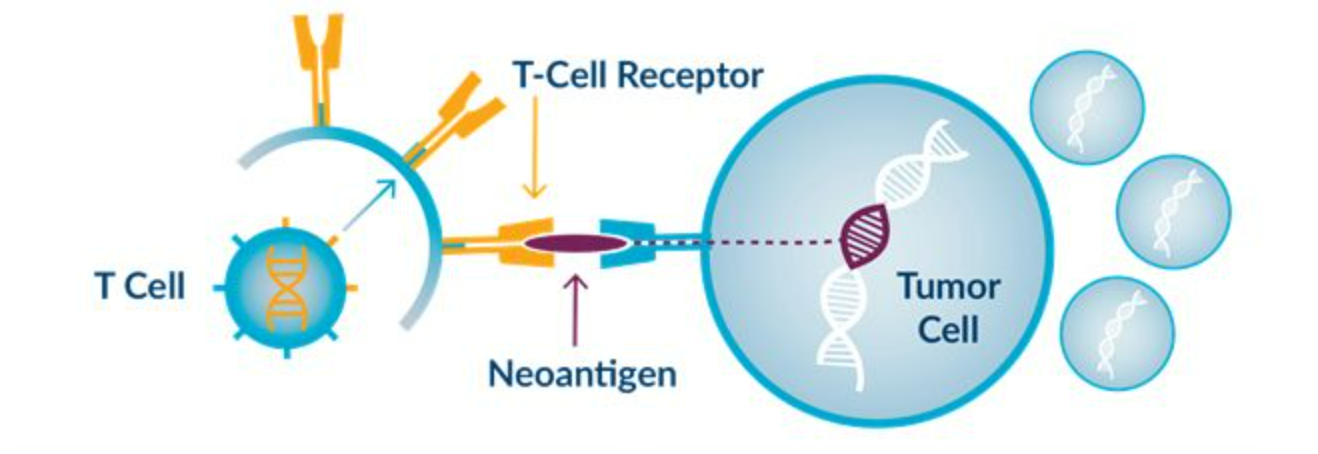
圖 | 腫瘤新抗原與 T 細(xì)胞
新抗原對個體患者的腫瘤具有高度特異性,基于觸發(fā)針對新抗原的T細(xì)胞反應(yīng)的個性化疫苗加速了腫瘤患者個體化免疫治療的發(fā)展。
新抗原的鑒定、篩選是基于新抗原的免疫療法的關(guān)鍵環(huán)節(jié)之一。BSI 在 2020 年首次報道了個體免疫肽組的個性化深度學(xué)習(xí)方法,以鑒定可以用于生產(chǎn)癌癥疫苗的新抗原,大大提高了發(fā)現(xiàn)具有免疫原活性的新抗原的效率。百蓁生物應(yīng)用此技術(shù)致力于以最短的項目周期為客戶提供發(fā)現(xiàn)新抗原服務(wù)。
百蓁生物的DeepImmu平臺為客戶提供一個從樣品處理到新抗原發(fā)現(xiàn)的完整解決方案:首先進(jìn)行免疫肽組分析, 再利用特有的 AI 算法發(fā)現(xiàn)新抗原,并對免疫原性進(jìn)行預(yù)測,為下游的細(xì)胞學(xué)靶點驗證提供更精準(zhǔn)的新抗原候選列表。
|
樣本類型 |
細(xì)胞 |
組織 |
血液 |
|
樣本最低需求量 |
107 |
50mg |
全血:10ml 血漿:5ml 血清:5ml |
|
樣本制備要求 |
細(xì)胞樣品需保持90%以上的活細(xì)胞率,同時防止支原體污染。 |
新鮮制備是為最佳;液氮速凍保存。注:防止血液污染 |
新鮮制備是為最佳;液氮速凍保存。注:防止出現(xiàn)溶血現(xiàn)象 |
|
樣本運輸要求 |
使用足量干冰運輸,期間避免凍融,盡量選用順豐快遞,防止樣品降解。 |
||
|
交付標(biāo)準(zhǔn) (報告內(nèi)容) |
1. 鑒定到的免疫肽列表 2. 質(zhì)控結(jié)果 3. 所有新生抗原及其對應(yīng)的蛋白信息列表 4. 所有新生抗原對應(yīng)蛋白功能富集分析 5. DeepImmu預(yù)測免疫原性排名前十新生抗原列表 6. 完整的實驗報告 |
||
2016 年來自德國馬普的科研人員MichalBassani-Sternberg 等在題為“Direct identification of clinically relevant neoepitopes presented on native human melanoma tissue by masss pectrometry”文章中,利用基于質(zhì)譜的免疫肽組分析和外顯子測序技術(shù)研究黑色瘤中的腫瘤新生抗原,最終發(fā)現(xiàn)了 11 條發(fā)生突變的免疫肽,并經(jīng)過Elispot 實驗驗證,發(fā)現(xiàn)其中 4 條具有免疫源性。文中分析使用的平臺為maxquant,是以外顯子測序數(shù)據(jù)作為database 進(jìn)行搜索,進(jìn)而發(fā)現(xiàn)突變的免疫肽。
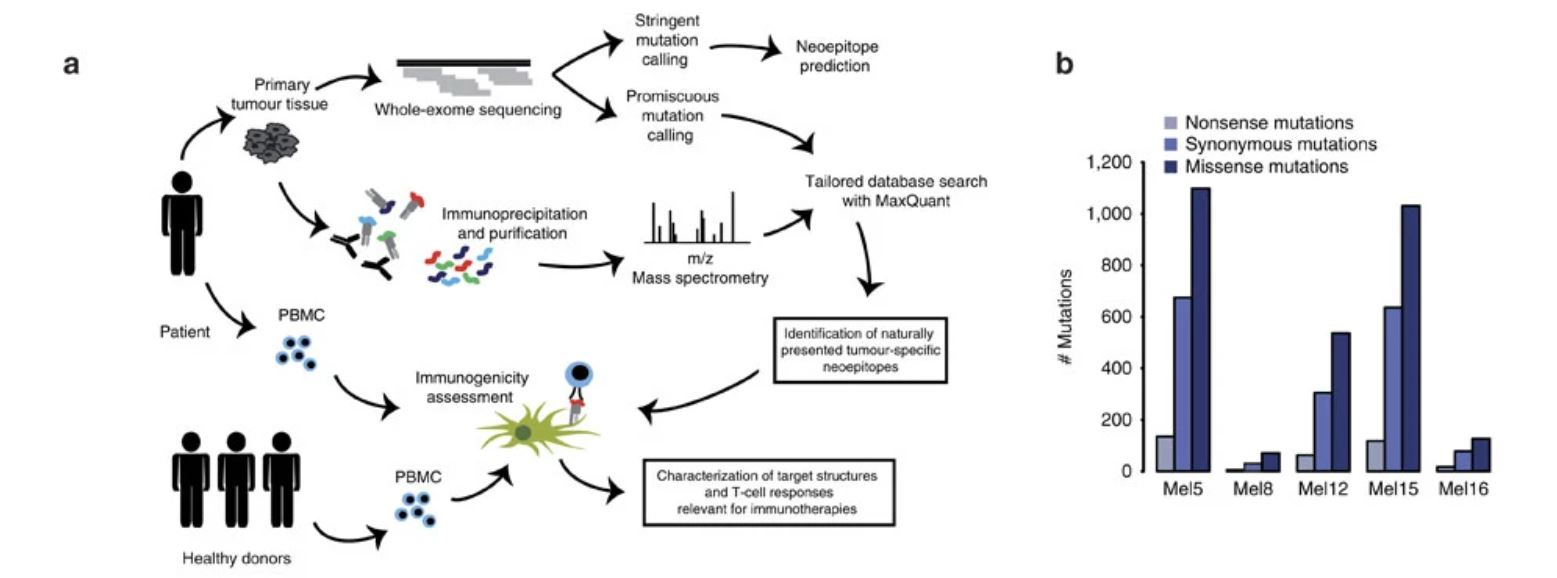
我們使用DeepImmu 平臺對文獻(xiàn)中的數(shù)據(jù)進(jìn)行de novo 從頭測序分析,不依賴于外顯子測序構(gòu)建database。其中多數(shù)突變的免疫肽均被鑒定到(見表 1)。并且我們還額外鑒定到一條突變的免疫肽是文章中沒有報道出來的。
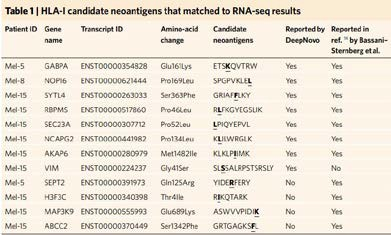
表 1 | 使用 DeepImmu 分析結(jié)果與文獻(xiàn)中分析結(jié)果對比
接下來我們是用DeepImmu 對文章報道的的突變的免疫肽段進(jìn)行免疫原性預(yù)測,并且與另外的免疫原性預(yù)測軟件
IEDB 進(jìn)行對比,根據(jù)預(yù)測的免疫原性強弱對其進(jìn)行排名,結(jié)果表明使用DeepImmu預(yù)測的結(jié)果與文中使用Elispot的實驗結(jié)果高度吻合,明顯高于IEDB 預(yù)測的結(jié)果準(zhǔn)確性,見表 2. 并且我們沒有檢測到的幾條免疫肽,在Elispot 免疫源性試驗中也是沒有免疫源性的。這就進(jìn)一步表明DeepImmu 平臺的準(zhǔn)確性。
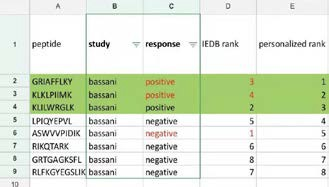
表 2 | 不同軟件免疫原性預(yù)測結(jié)果比較
Response:文章中使用 Elispot 驗證免疫原性結(jié)果;IEDB rank:使用 IEDB 預(yù)測免疫源性強弱排名;personalized rank:使用DeepImmu 預(yù)測免疫源性強弱排名



