多組學揭示腸道微生物群失調加重腹主動脈瘤

腹主動脈瘤(AAA)是一種隱蔽的、致命的血管疾病,缺乏有效的非手術治療干預手段。AAA的發病機制非常復雜,中性粒細胞及其釋放的中性粒細胞胞外誘捕網(NETs)被認為可以促進AAA的進展。大量研究表明,腸道微生物及其代謝產物在宿主機體穩態調控和疾病發生發展中發揮關鍵作用。然而,AAA患者的腸道微生物群是否異常、腸道微生物失調與AAA之間的因果關系及其潛在機制仍未闡明。
2022年10月,山東大學齊魯醫院張群業教授、張澄教授和山東第一醫科大學附屬省立醫院王哲教授團隊在Cell子刊: Cell Host & Microbe (IF: 31.316)上發表題為“Gut microbiome dysbiosis contributes to abdominal aortic aneurysm by promoting neutrophil extracellular trap formation”的研究文章。通過16S多樣性、宏基因組與代謝組學技術聯合,發現AAA患者腸道微生物組成存在明顯異常,如Roseburia intestinalis豐度在患者中下降。代謝譜在健康個體和患者中也有明顯改變,如丁酸含量降低、幾種短鏈脂肪酸(SCFAs)的水平顯著升高。為了研究其中機制,還進行了糞菌移植(FMT)和體內外功能實驗,驗證與AAA病情發展密切相關。另外,中性粒細胞耗竭能顯著減輕移植AAA患者糞便的AAA小鼠的病情。中科新生命為其提供了 非靶代謝組學和靶向短鏈脂肪酸檢測的技術服務。

研究材料
33例腹主動脈瘤患者和31例健康對照組;野生型和載脂蛋白E基因敲除 (ApoE-/-)小鼠
技術路線
步驟1:AAA患者的腸道微生物群失調;
步驟2:AAA患者腸道微生物群功能和共生網絡的顯著變化;
步驟3:腸道微生物群代謝特征顯著改變并與 AAA患者的病情相關;
步驟4:顯著增加中性粒細胞浸潤和NET形成并促進AAA發展;
步驟5:R. intestinalis及其代謝物丁酸在體內抑制中性粒細胞浸潤和 NET 形成并改善AAA。
研究結果
1. AAA患者的腸道微生物群失調
首先,研究人員對33例腹主動脈瘤患者和31例健康對照組的糞便樣本進行了宏基因組分析。結果表明,與健康個體相比,AAA患者的腸道微生物群存在明顯失調,細菌占腸道微生物群的 98.05%。在屬水平上,包括細菌、古細菌和病毒在內的許多腸道微生物群的豐度在AAA患者中發生了顯著變化。在物種水平上,許多產生 SCFAs的細菌,如高豐度的丁酸產生菌Roseburia intestinalis等多種有益菌的豐度明顯降低,并且與瘤直徑負相關。除了細菌外,AAA患者腸道中其他微生物的豐度也發生了顯著變化。許多病毒的豐度,如志賀氏病毒pSf1,埃希氏病毒Bp4等,在AAA患者中明顯高于健康人群。這些結果表明,一些病毒、古生菌或真菌也可能與AAA的發生有關。
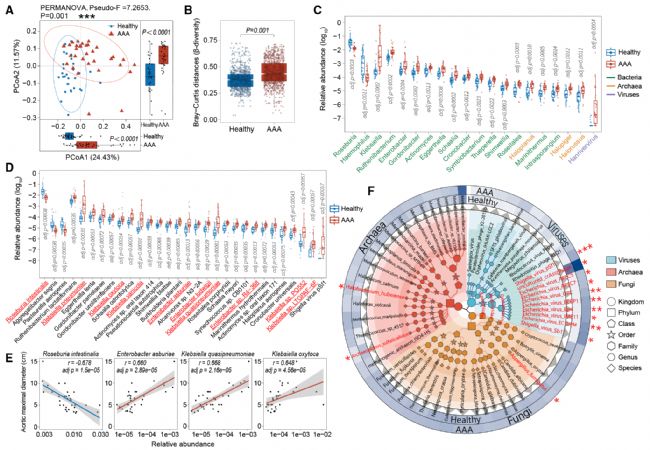
2. AAA患者腸道微生物群功能和共生網絡的顯著變化

3. 腸道微生物群代謝特征顯著改變并與AAA患者的病情相關
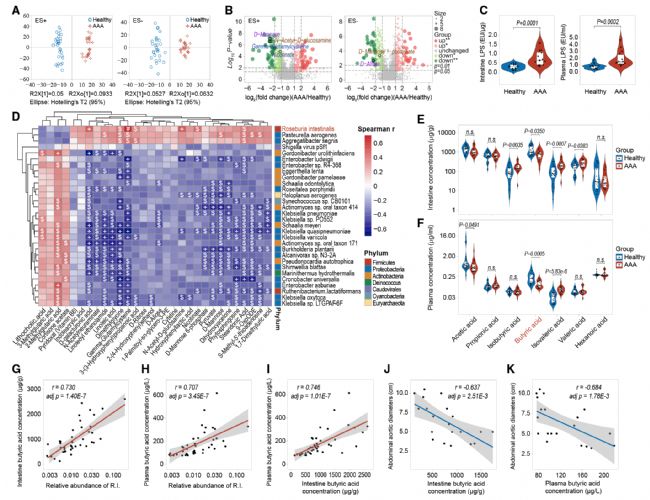
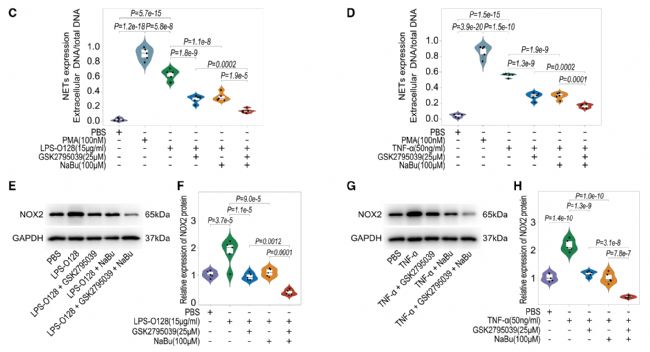
4. 顯著增加中性粒細胞浸潤和NET形成并促進AAA發展
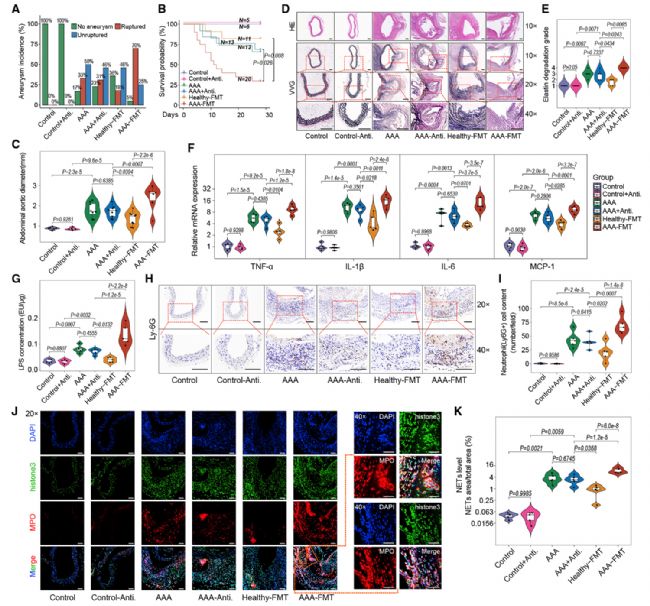
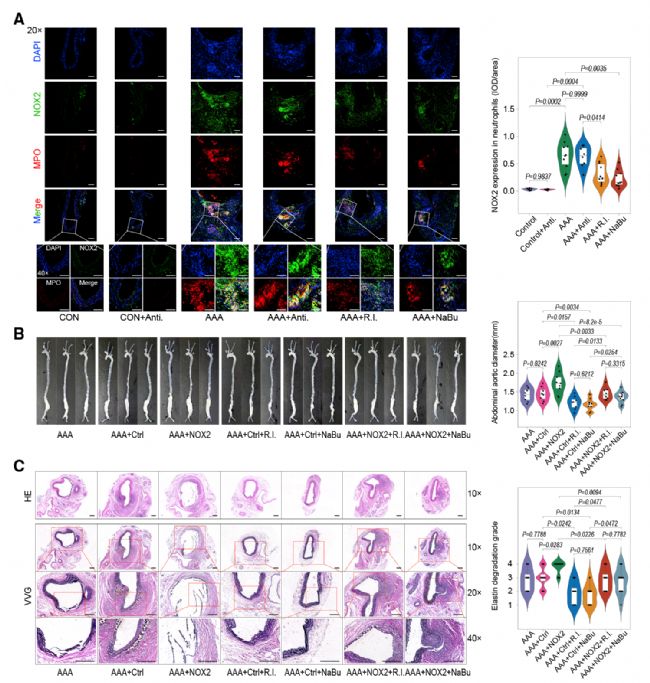
5. R. intestinalis及其代謝物丁酸在體內抑制中性粒細胞浸潤和NET形成并改善AAA
研究者的上述結果已表明R. intestinalis可能對AAA的發展具有重要影響。因此,接下來的研究重點放在了這種益生菌上。進一步的分析表明,R. intestinalis及其代謝物丁酸鹽可以顯著改善體內AAA的多種病理異常,包括中性粒細胞浸潤增強、NET形成、炎癥、VSMC向合成表型轉變和彈性纖維破壞,從而減輕AAA。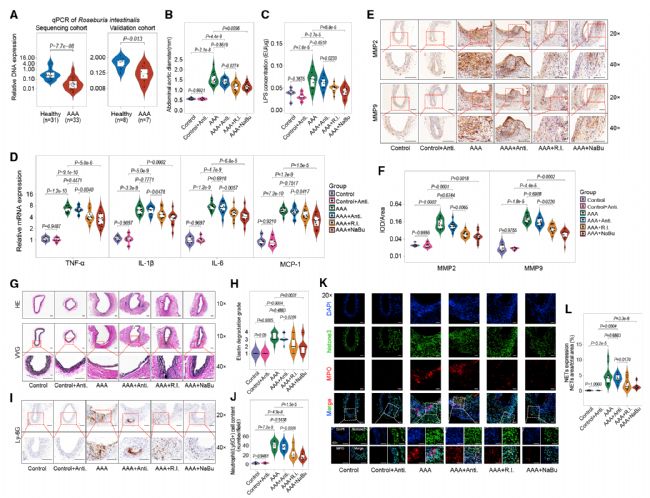
小結
綜上所述,研究揭示了AAA患者的腸道生態失調,并證實腸道菌群失調是AAA的重要原因。Roseburia intestinalis及其代謝物丁酸鹽可顯著抑制腹主動脈中性粒細胞浸潤和NET形成,從而改善AAA的多種病理變化,有效緩解AAA進展。研究者們的發現也促進了對腸道微生物和宿主免疫以及疾病發展的理解。





