ÞDä+ĩ°°Ũ―M·ÖÎö―ŌĘūMUP1pÝpČŲ|ūWŠžĪĩÄŨũÓÃ


ŅÐūŋēÄÁÏ
ÐĄĘóļÎÅK―MŋĄĒŅŠĮåĄĒÄōŌšĄĒÐĄĘóÔīúļΞ°ûĄĒAML12ž°ûĄĒHepG2ž°û
žžÐg·ū
ē―óE1ĢšÔÚNAFLDÐĄĘóÄĢÐÍÖÐĢŽļÎ―MŋÖÐMUPĩ°°Ũï@ÖøpÉŲĢŧ
ē―óE2ĢšÔÚČŲ|ūWŠžĪÏÂĢŽļΞ°ûÖÐMUP1ĩ°°Ũąíß_šÍ·ÖÃÚpÉŲĢŧ
ē―óE3ĢšMUP1īĖžĪļΞ°ûÖÐĩÄČŲ|ūWâ}ÁũģöēĒÕT§žąÐÔČŲ|ūWŠžĪ·īŠĢŧ
ē―óE4ĢšMUP1ļÉîAÄÜōŌýÆðļΞ°ûîAßmŠÓÚČŲ|ūWŠžĪĢŽßMķøū―âËÎïŌýÆðĩÄČŲ|ūWŠžĪž°ČŲ|ūWŠžĪŌýÆðĩÄŌČuËØĩÖŋđĄĢ
ŅÐūŋ―Yđû
1. NAFLDÐĄĘóļÎÅKÖÐMUPĩ°°ŨpÉŲ
ÉúĀíÖļËzy―Yđû°lŽFNAFLDÐĄĘóąíŽFģöówÖØß^ķČÔöžÓĄĒļÎÅKÅcówÖØšÍÖŽ·ūÅcówÖØĩÄąČÂĘÔöžÓĢŽŌÔž°ļÎÅKļĘÓÍČýõĨšŽÁŋï@ÖøÔöžÓĄĢéÁËßMŌŧē―Ė―ÓNAFLDÐĄĘóļÎÅKČĩ°°ŨŲ|ĩÄŨŧŊĢŽŨũÕßēÉÓÃÁËĩ°°ŨŲ|―MW·ÖÎöĢŽ―Yđûï@ĘūNAFLDÐĄĘóĩÄķā·NMUPÐÍĩÄï@ÖøÏÂ―ĩĢŽÆäÖÐMUP1ÐÍŋÉÄÜĶīúÖxØŦIŨîīóĄĢß@ÐĐĩþąíÃũMUPsĢŽÓČÆäĘĮMUP1ĢŽŋÉÄÜĘĮ ĒÅcNAFLDīúÖxÕ{đĩÄÖØŌŠŌōŨÓĄĢ
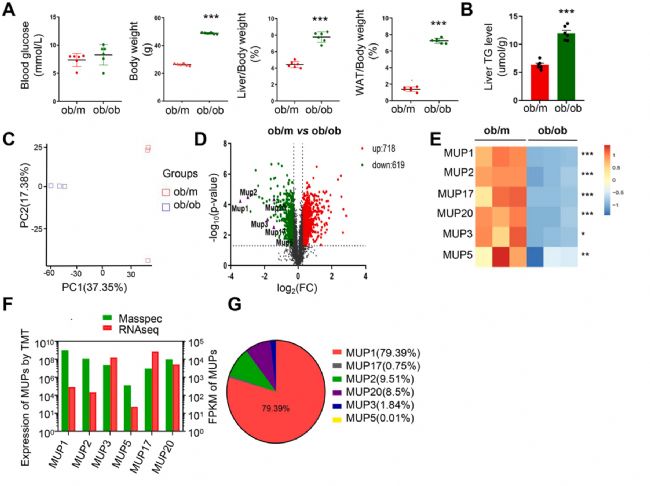
D1 NAFLDÐĄĘóÉúĀíÖļËž°ĩ°°Ũ―Mzy
2. NAFLDÐĄĘóļÎÅKČŲ|ūWŠžĪ·īŠĘÜp
KEGG·ÖÎöï@ĘūĢŽ“ČŲ|ūWÖÐĩÄĩ°°ŨŲ|žÓđĪ”Íū―ï@ÖøØSļŧĄĢNAFLDÐĄĘóÖÐĢŽÎīÕÛŊBĩ°°ŨŠīðĢĻUPRĢĐšÍČŲ|ūWÏāęPĩ°°Ũ―ĩ―âĢĻERADĢĐÍū―ĩÄąíß_ÄĢĘ―°lÉúÁËÃũï@ļÄŨĄĢĮŌWB―Yđûï@ĘūĢŽÔÚNAFLDÐĄĘóĩÄļÎÅKÖÐĢŽIRE1αšÍPERKĩÄËŪÆ―ï@ÖøÔöžÓĢŽķøp-eIF2αĄĒATF4šÍBiPĩÄËŪÆ―ï@Öø―ĩĩÍĢŽß@ąíÃũÔÚīúÖxÎÉyšÍļÎÅKČŲ|ūWŠžĪ·īŠÖÐUPRÐÅĖʧÕ{§ÖÂČŲ|ūWØúÔöžÓĄĢß@ÐĐĩþąíÃũĢŽÔÚNAFLDÐĄĘóÄĢÐÍÖÐĢŽļÎÅKČŲ|ūWŠžĪ·īŠĘÜp ĄĢ
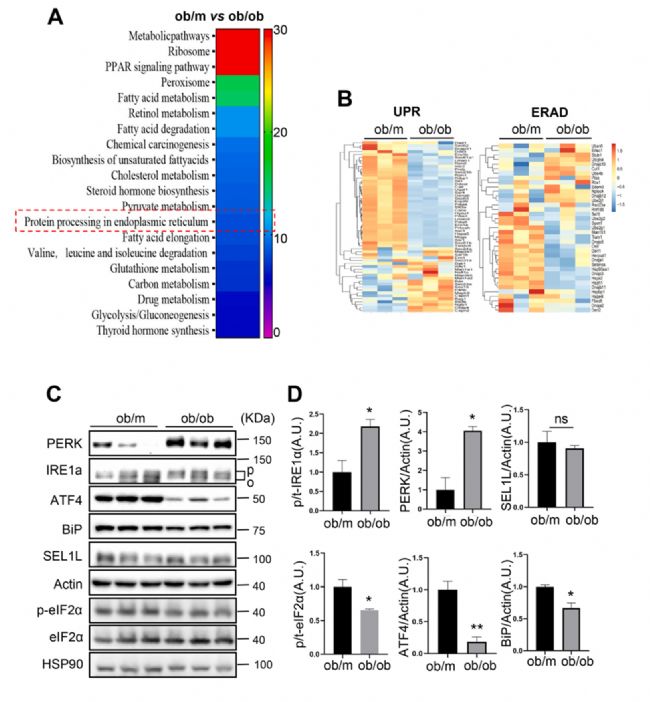
D2 NAFLDÐĄĘóđĶÄÜÍĻ··ÖÎö
3. ČŲ|ūWŠžĪÏÂļΞ°ûMUP1ĩÄąíß_―ĩĩÍ
―ÓÏÂíĢŽŨũÕßĒNAFLDÐĄĘóšÍĶÕÕÐĄĘóļđĮŧŨĒÉäŌÂÃđËØĢĻTmĢŽŌŧ·NČŲ|ūWŠžĪÕT§ĐĢĐŧōĩČÁŋDMSOŌÔ―ĻÁĒļÎÅKČŲ|ūWŠžĪÐĄĘóÄĢÐÍĢŽĩ°°ŨŲ|zy―Yđûï@ĘūMUPsĩÄËŪÆ―ÔÚļÎÅKČŲ|ūWŠžĪÄĢÐÍÖÐï@Öø―ĩĩÍĄĢWB·ÖÎöŨCÁËMUP1ÔÚļÎÅKÖÐĩÄîËÆąíß_ÄĢĘ―ĄĢŌōīËĢŽMUPsąŧčbķĻéīúÖxšÍČŲ|ūWŠžĪ·īŠĩ°°ŨĢŽß@ąíÃũMUPsŋÉÄÜĘĮNAFLDÖÐČŲ|ūWŠžĪšÍīúÖxĩÄÔÚÂÏĩĄĢ
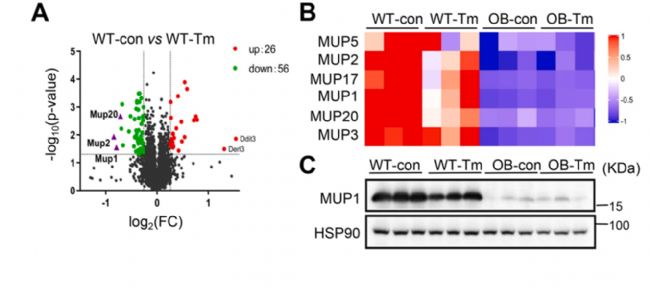
D3 ļΞ°ûÖÐMUPĩÄąíß_ÄĢĘ―
4. ČŲ|ūWŠžĪÕT§ļΞ°ûČŲ|ūWÖÐMUP1ūÛžŊ
éÁË―âQMUP1íŠČŲ|ūWŠžĪķø―ĩĩÍĩÄCÖÆĢŽĶļÎÅKĮÐÆŽßMÐÐÃâŌßÉđâČūÉŦŌÔī_ķĻMUP1ÔÚļÎÅKÖÐĩÄ·ÖēžĄĢđēūÛ―đï@ÎĒįR·ÖÎöï@ĘūĢŽÅcĶÕÕÐĄĘóÏāąČĢŽMUP1ąĢÁôÔÚTmÐĄĘóĩÄļΞ°ûČŲ|ūWÖÐĄĢßMŌŧē―ąíÃũČŲ|ūWŠžĪÏÂMUP1ÔÚČŲ|ūWÖÐĩÄþÁôÔöžÓĢŽß@ēŋ·Ö―âáÁËž°ûÖÐģÉĘėMUP1ĩÄpÉŲĄĢ
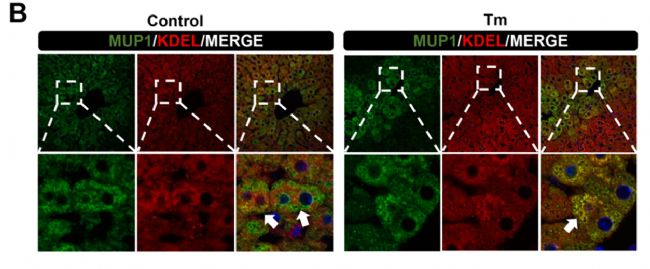
D4 MUP1ÔÚļÎÅKÖÐĩÄ·Öēž
5. MUP1īĖžĪļΞ°ûČŲ|ūWÖÐâ}ëxŨÓÍâÁũēĒÕT§žąÐÔČŲ|ūWŠžĪ
ÓÃMUP1ĖĀíÔīúļΞ°ûēĒßMÐÐRNAyÐōĢŽGSEA·ÖÎöï@ĘūĢŽ“â}ÐÅĖÍĻ·”ï@ÖøļŧžŊĢĻD5BĢĐĄĢÓÉÓÚâ}·BĶČŲ|ūW·BšÍž°ûÃüß\ÖÁęPÖØŌŠĢŽŌōīËĢŽŨũÕßÍÆyMUP1ŨũéČŲ|ūWŠžĪ·īŠĩ°°ŨĢŽŋÉÄÜÍĻß^·īð
ĒÅcČŲ|ūWŠžĪĩÄÕ{đĄĢéÁËßMŌŧē―ŅÐūŋMUP1ĶļÎÅKČŲ|ūWŠžĪĩÄÓ°íĢŽÓÃķūšúĖ}ē·ËØĢĻthapsigarginĢŽTgĢĐŨũéÕ{đCa2+âķČĩÄęÐÔĶÕÕĄĢ―Yđûï@ĘūĢŽMUP1ĖĀíËērīĖžĪČŲ|ūWŠžĪÍū―ĄĢÖĩĩÃŨĒŌâĩÄĘĮĢŽMUP1ĶČŲ|ūWŠžĪĩÄÓ°íÅcTgÏāËÆĢŽąíÃũMUP1ĶCa2+·BĩÄÔÚŨũÓÃĄĢķøÔÚoCa2+ČÜĐÖÐÓÃMUP1ĖĀíĢŽCa2+ÄERÁũģöĢŽï@ÖøÔöžÓÁË°û{Ca2+âķČĄĢß@ÐĐĩþąíÃũĢŽMUP1īĖžĪļΞ°ûÖÐĩÄČŲ|ūWâ}ëxŨÓÍâÁũēĒÕT§žąÐÔČŲ|ūWŠžĪ·īŠĄĢ
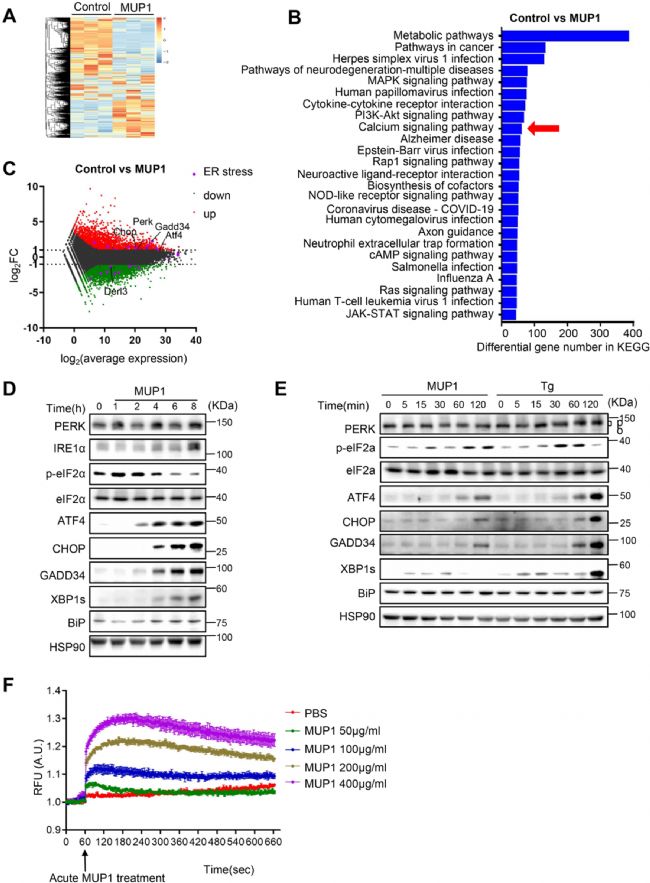
D4 MUP1ÔÚļÎÅKÖÐĩÄ·Öēž
5. MUP1īĖžĪļΞ°ûČŲ|ūWÖÐâ}ëxŨÓÍâÁũēĒÕT§žąÐÔČŲ|ūWŠžĪ
ÓÃMUP1ĖĀíÔīúļΞ°ûēĒßMÐÐRNAyÐōĢŽGSEA·ÖÎöï@ĘūĢŽ“â}ÐÅĖÍĻ·”ï@ÖøļŧžŊĢĻD5BĢĐĄĢÓÉÓÚâ}·BĶČŲ|ūW·BšÍž°ûÃüß\ÖÁęPÖØŌŠĢŽŌōīËĢŽŨũÕßÍÆyMUP1ŨũéČŲ|ūWŠžĪ·īŠĩ°°ŨĢŽŋÉÄÜÍĻß^·īð ĒÅcČŲ|ūWŠžĪĩÄÕ{đĄĢéÁËßMŌŧē―ŅÐūŋMUP1ĶļÎÅKČŲ|ūWŠžĪĩÄÓ°íĢŽÓÃķūšúĖ}ē·ËØĢĻthapsigarginĢŽTgĢĐŨũéÕ{đCa2+âķČĩÄęÐÔĶÕÕĄĢ―Yđûï@ĘūĢŽMUP1ĖĀíËērīĖžĪČŲ|ūWŠžĪÍū―ĄĢÖĩĩÃŨĒŌâĩÄĘĮĢŽMUP1ĶČŲ|ūWŠžĪĩÄÓ°íÅcTgÏāËÆĢŽąíÃũMUP1ĶCa2+·BĩÄÔÚŨũÓÃĄĢķøÔÚoCa2+ČÜĐÖÐÓÃMUP1ĖĀíĢŽCa2+ÄERÁũģöĢŽï@ÖøÔöžÓÁË°û{Ca2+âķČĄĢß@ÐĐĩþąíÃũĢŽMUP1īĖžĪļΞ°ûÖÐĩÄČŲ|ūWâ}ëxŨÓÍâÁũēĒÕT§žąÐÔČŲ|ūWŠžĪ·īŠĄĢ
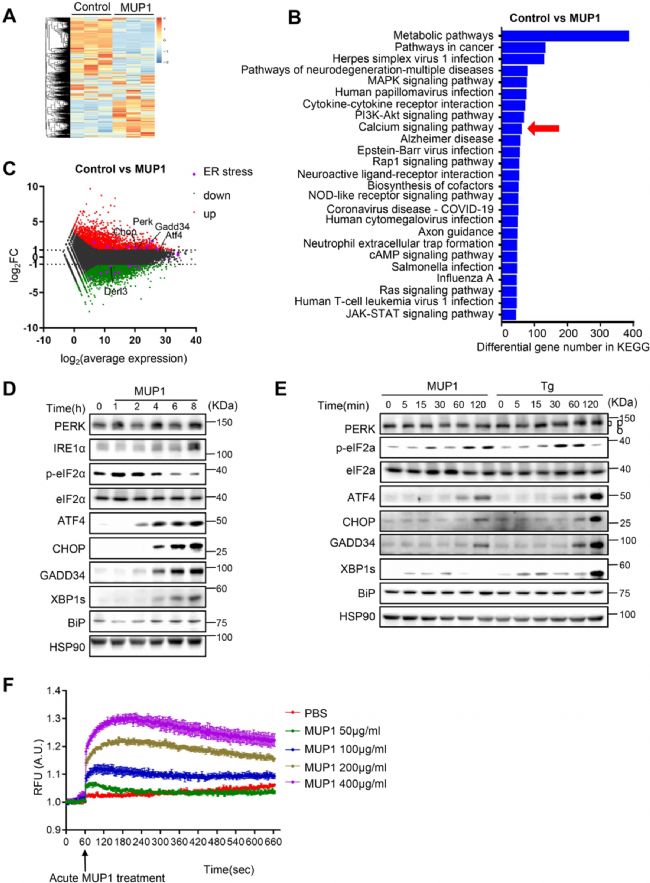
D5 MUP1ĶļÎÅKČŲ|ūWŠžĪĩÄÓ°í
6. MUP1îAĖĀíŌÖÖÆĩ°°ŨŲ|šÏģÉēĒpÝpļΞ°ûČŲ|ūWŠžĪšÍŌČuËØĩÖŋđ
éÁËßMŌŧē―ŅÐūŋMUP1ÔÚķĖšīĖžĪČŲ|ūWŠžĪÖÐĩÄÉúĀíŌâÁxĢŽĒÔīúļΞ°ûÓÃMUP1îAĖĀíšóÓÃTmĖĀíÕT§ŠČŲ|ūWŠžĪĄĢWBšÍÞDä―M―YđûąíÃũĢŽTmï@ÖøÔöžÓÁËČŲ|ūWŠžĪËÖūÎïĩÄĩ°°ŨŲ|ËŪÆ―ĢŽ°üĀĻGADD34ĄĒATF4ĄĒCHOPĄĒXBP1sšÍp-eIF2αĢŽķøMUP1îAĖĀíŋÉŌÖÖÆERŠžĪĄĢ―ÓÏÂíĢŽŨũÕßÔuđĀÁËŌÖÖÆļÎÅKČŲ|ūWŠžĪĶŌČuËØ·īŠĩÄÓ°íĄĢMUP1îAĖĀíž°ûĘÜĩ―ČŲ|ūWŠžĪrĢŽAktï@ÖøÔöĢŽČŲ|ūWŠžĪËÓÎïï@ÖøpČõĢŽß@ąíÃũŌČuËØÃôļÐÐÔšÍļÎČŲ|ūWŠžĪĩÃĩ―ļÄÉÆĄĢÔĩþąíÃũĢŽMUP1îAĖĀíÔÚówÍâpÝpÁËļÎÅKČŲ|ūWŠžĪšÍČŲ|ūWŠžĪÕT§ĩÄŌČuËØĩÖŋđĄĢ
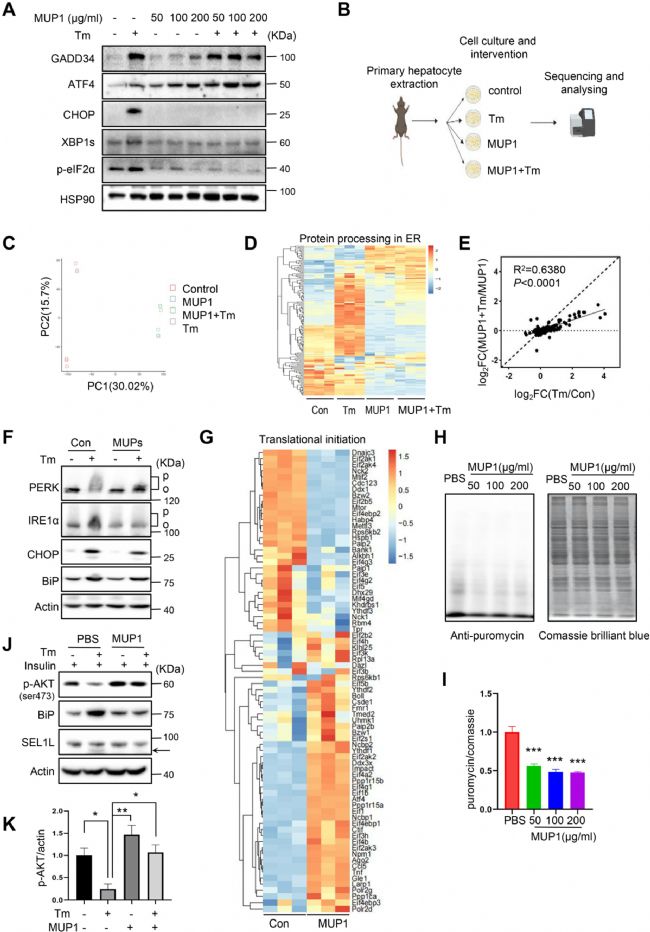
D6 MUP1îAĖĀípÝpÁËļΞ°ûČŲ|ūWŠžĪšÍŌČuËØĩÖŋđ
7. MUP1îAĖĀípÝpTmÕT§ĩÄļÎÅKČŲ|ūWŠžĪ
éÁËÔuđĀMUP1ÔÚówČĩÄēĄĀíÉúĀíŨũÓÃĢŽÓÃMUP1îAĖĀíÐĄĘóČŧšóļđĮŧŨĒÉäTmŌÔ―ĻÁĒžąÐÔČŲ|ūWŠžĪÄĢÐÍĢŽTmĖĀí§ÖÂÃũï@ĩÄļÎÅKļĘÓÍČýõĨ·eūÛšÍŋÕÅÝŧŊĢŽMUP1îAĖĀí―MÓÐËųļÄÉÆĢŽ―YđûąíÃũMUP1îAĖĀípÝpÁËTmÕT§ĩÄß^ķČļÎÅKÖŽ·ūŨÐÔĄĢÍŽrĢŽŨũÕßßŅÐūŋÁËÄIÅKÖÐĩÄČŲ|ūWŠžĪ·īŠĄĢÓÐČĪĩÄĘĮĢŽMUP1îAĖĀíï@ÖøpÝpÁËTmÕT§ĩÄÄIČŲ|ūWŠžĪĢŽß@ąíÃũMUP1ĶówČČŲ|ūWŠžĪ·īŠĩÄÓ°í ĄĢ
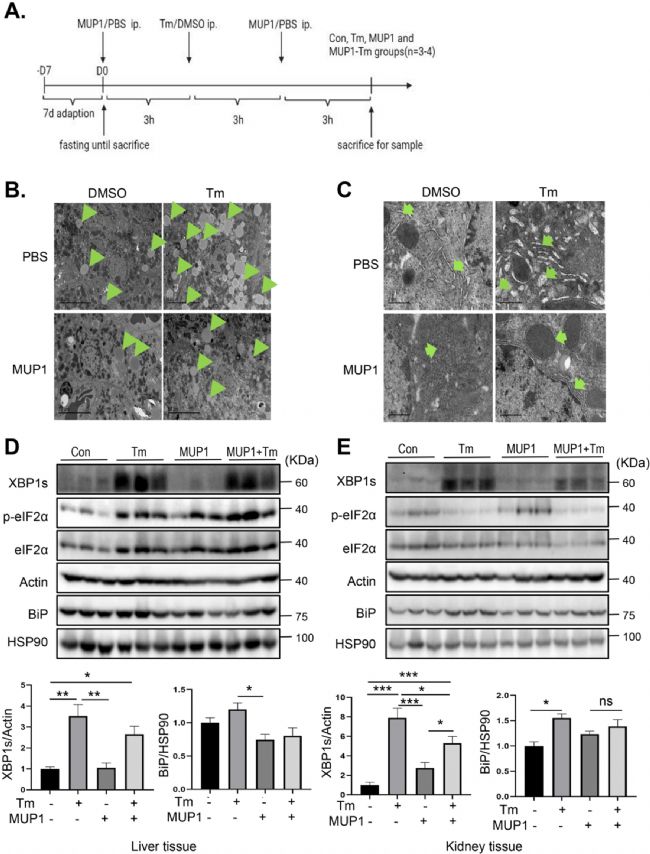
D7 MUP1ÔÚówČĩÄēĄĀíÉúĀíŨũÓÃ
ÐĄūÐĄ―Y
ÔÚß@íŅÐūŋÖÐĢŽŨũÕßĖáđĐÁËļÎÅKMUPsï@Öø―ĩĩͧÖÂČŲ|ūWŠžĪĘÜpĩÄŨCþĄĢMUP1ŨũéMUPžŌŨåÖÐŨîØSļŧĩÄģÉTĢŽÓÉČŲ|ūWšÏģɚ͞ÓđĪĢŽËüĘÜĩ―ČŲ|ūWŠžĪĩÄØÕ{đĄĢÄCÖÆÉÏÖvĢŽļÎÅKČŲ|ūWŠžĪ§ÖÂMUP1ÐÎģÉūÛžŊówēĒąŧĀ§ÔÚČŲ|ūWÖÐĢŽÄķøpÉŲMUP1ĩÄ·ÖÃÚĄĢīËÍâĢŽÔÚļΞ°ûÖÐŅaģäÖØ―MMUP1ÔöžÓÁËČŲ|ūWâ}ëxŨÓÍâÁũÖÁ°û{ÖÐĢŽēĒķĖšÕT§îAßmŠČŲ|ūWŠžĪĢŽß@ÓÐÖúÓÚļΞ°ûÍĻß^ŌÖÖÆĩ°°ŨŲ|šÏģÉípÝpŧŊWÕT§ĩÄČŲ|ūWŠžĪšÍČŲ|ūWŠžĪÕT§ĩÄŌČuËØĩÖŋđĢŽąíÃũNAFLDĩÄÔÚÖÎŊ°ÐücĄĢ
- ËŪŲ|·ÖÎöÏĩ―yōĘŌÔOÓŌÔ―â
- ―ŌĘūÐĄĘóÅßĖĨÄļÔī-šÏŨÓÞDQß^ģĖÖÐĩÄRNA m6AÓB
- Ξ°ûž°ŋÕégķā―MW―ŌĘūAPOE4ÔÚËĨĀÏĄĒÉņ―ŅŨ°YšÍ°Ē ÆšĢÄŽ°YĩÄCÖÆ
- ĀûÓÃACSL4īŲßMÉņ―ŅŨ°YÐÂCÖÆĩÄŅÐūŋ
- Int J Mol SciĢšķā―MW―ŌĘūMCT2ÏÞÖƷΰĐÐĄĘóÄĢÐÍÖÐĩÄÄ[ÁöÉúéL
- ÄcĩĀūúČš-°ÐÆũđŲķā―MWĢš16sšÍ·Į°ÐīúÖx―MWzyŠÓÃÓÚËŪĖKĖĮŅÐūŋ
- ÖÐátówŲ|WĩÄÉúĀíWŧųĩA―é―B
- ļÉØ·ÖÏí--ļßÍĻÁŋyÐōÔĘžĩþÉÏũ―ĖģĖ
- ÁŋĘSPRŧĨŨũzy·þÕĢšÐÔrąČéšÎČįīËÖŪļßĢŋ
- šžÖÝWĘĒsâߥ°2023ÖÐøÄęķČßxđÍÖũĄą
- ĮÚÏčŋÆWxÆũĘÚā·þÕđĪģĖÅāÓþŨhÔÚüSÉ―íĀûÅeÞk
- ÖÐŋÆÐÂÉúÃü3Ô°ląíÎÄÕÂ37ÆŠĢŽÆ―ūųÓ°íŌōŨÓ8.12·ÖĢĄ
- ÖÐŋÆÐÂÉúÃüHL2400ļßÍĻÁŋ°ÐÏōÖŽŲ|―MÉýž-"ÖŽ"ĩÃíÓÐ
- īšÅŊŧĻé_,ļÐķũÏā°é--ÖÐŋÆÐÂÉúÃüÉîķČŋÕégīúÖx―MīóīŲ
- ÖÐŋÆÐÂÉúÃü2023APTîIÓō―âQ·―°ļČŦøŅēÖvČŦÃæĒÓ
- ÖÐŋÆÐÂÉúÃü"ŅŠŌšīúÖx―M-CellĩČļß·ÖÎÄÕÂŌŧŨũ·ÖÏíþ"





