īóßBŧŊWÎïĀíŅÐūŋËųĮäđâėÍFę ŽFĶÍŲŌšËáĖĮæßB―ÓŪówĩÄūŦī_ ^·Ö
īóßBŧŊWÎïĀíŅÐūŋËųĮäđâėÍFę ŽFĶÍŲŌšËáĖĮæßB―ÓŪówĩÄūŦī_
^·Ö
ąūÎÄíÔīĢšÖÐøŋÆWÔšīóßBŧŊWÎïĀíŅÐūŋËųĢŧÞDÝdŨÔÖÐŋÆÔšÖŪÂ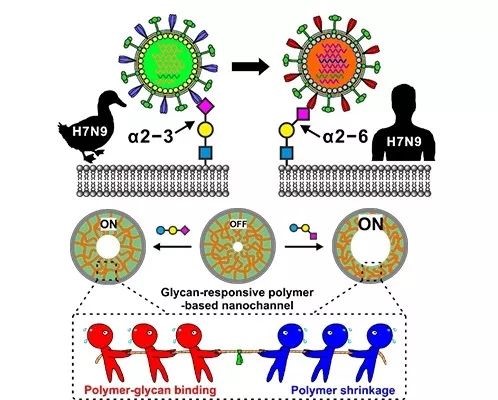
ÖÐøŋÆWÔšīóßBŧŊWÎïĀíŅÐūŋËųÉúÎï·ÖëxÅc―įÃæ·ÖŨÓCÖÆÐÂĖØ ^―MĢĻ18T7―MĢĐŅÐūŋTĮäđâėÍFę ĢŽÍĻß^ÖþŧųÓÚÉúÎï·ÖŨÓíŠÐÔūÛšÏÎïĩÄ·ÂÉúëxŨÓÍĻĩĀĢŽŽFÁËĶÍŲŌšËáĖĮæßB―ÓŪówĩÄūŦī_ŨReÅc ^·ÖĢŽÍŽr―ŌĘūÁËŌŧ·NŧųÓÚ“ēĐÞÄ”ĩÄÞDŨCÖÆĄĢ
ÍŲŌšËáĖĮÍĻģĢŌÔα2-3ŧōα2-6·―Ę―ßB―ÓÔÚĖĮæÄĐķËĄĢÍŲŌšËáĖĮæ·ÖēžÔÚēļČéÓÎïž°ûŧōŌŧÐĐ·ÖÃÚĩ°°ŨŲ|ąíÃæĢŽß@·NŨîÍâķËÎŧÖÞ°ÆäV·šĩÄ·ÖēžÐÔĘđĩÃÍŲŌšËáĖĮæÔÚēĄķūļÐČūĄĒÃâŌß튥Ē°Đ°Y°lÕđĩČß^ģĖÖÐÆðÖøÖØŌŠŨũÓÃĄĢČŧķøÓÉÓÚÍŲŌšËáĖĮæ―MģÉÍësĢŽßB―ÓÐÎĘ―ķāÓĢŽÉõÖÁīæÔÚßB―ÓŪówĢŽ§ÖÂÆäŨRečbķĻž°―Y―âÎöīæÔÚšÜīóëyķČĄĢ
ÔFę ĒūßÓÐĖĮŨReíŠÐÔĩÄūÛšÏÎï―ÓÖĶĩ―ž{ÃŨÍĻĩĀČēŋĢŽĀûÓÃēŧÍŽĖĮæÕT§ūÛšÏÎïĘÕŋsĢŽÄķø§Öž{ÃŨÍĻĩĀēŧÍŽģĖķČĩÄ“OFF-ON”ŨŧŊĢŽŌÔž°ÝģöëxŨÓëÁũĩÄŋÉŨReŨŧŊĢŽŽFēŧÍŽĖĮææ―ÓŪówĩÄŨReÅc ^·ÖĄĢß@ŌŧđĪŨũßMŌŧē―ÍØÕđÁË·ÂÉúëxŨÓÍĻĩĀÆũžþÔÚÉúÎï·ÖŨÓŨReũļÐÖÐĩÄŠÓÃĢŽÓČÆäĘĮÔÚÍësĖĮæ·ÖŨÓĩÄŨRešÍ―Y―âÎö·―ÃæŨöģöÁËĖ―ËũĢŽéšóĀmŽFÍësĖĮæηÖŨÓŨReÅc―âÎöŨöÁËä|ĄĢÍŽrŅÐūŋ―MßĀûÓÃÖĮÄÜūÛšÏÎïĩÄÔOÓĀíÄîĢŽ―ĻÁËâ}ëxŨÓŨÔÕ{ŋØĩÄ·ÂÉúëxŨÓÍĻĩĀĢŽŌÔž°hÁŨËáÏŲÜÕÕ{ŋØĩÄž{ÃŨëxŨÓÍĻĩĀĄĢ
ÏāęPģÉđûŌÔEdge ArticleÐÎĘ―°ląíÔÚÓĒøŧĘžŌŧŊWþĄķŧŊWŋÆWĄ·ÉÏĄĢÔđĪŨũĩÃĩ―øžŌŨÔČŧŋÆWŧų―ðÃæÉÏíÄŋĄĒīóßBŧŊÎïËųÐÂĖØ ^―MĒÓŧų―ðĄĒÅdß|ÓĒēÅÓĩČĩÄÖ§ģÖĄĢ
ÎÄÖÐŨũÕßÍĻß^EDCÅžÂ―ðąíÃæđĖķĻŧųŌŌËáËųąĐÂķģöĩÄôČŧųĢŽĒūÛšÏÎïGlc-PEIÐÞïĩ―QCM-DÐūÆŽąíÃæĢŽÐÎģÉŌŧÓūÛšÏÎïÄĪĄĢČŧšóĢŽĘđÓÃQSenseĘŊÓĒū§ówÎĒĖėÆ―xÆũĢŽŅÐūŋÁËūÛšÏÎïGlc-PEIÅcÄŋË·ÖÎöÎïĢĻÍŲŌšËáÎĖĮšÍÉ·NÍŲŌšËáĖĮæĢš2-3ĖĮæšÍ2-6ĖĮæĢĐÖŪégĩÄ―YšÏÓHšÍÁĶž°ÆäÅcūÛšÏÎïÏóŨŧŊÖŪégĩÄęPÏĩĄĢQCM-Dō―YđûÄîlŌÆšÍÄÜÁŋšÄÉĒÆŦŌÆÉ·―ÃæŨCÃũÁËūÛšÏÎïGlc-PEIšÍ·ÖÎöÎïĩÄ―YšÏÓHšÍÁĶÅcūÛšÏÎïGlc-PEIŨÔÉíĘÕŋs·ųķČÖŪégīæÔÚØÏāęPęPÏĩĢŽžī―YšÏ§ÖÂūÛšÏÎïÐĄ·ųķČĘÕŋsĢŽķøÝ^ČõĩÄ―YšÏ s§ÖÂīó·ųķČĩÄĘÕŋsĄĢGlc-PEIūÛšÏÎïÄĪĶēŧÍŽ·ÖÎöÎïĢĻNeu5AcĢŽ2-6ĖĮæĢŽ2-3ĖĮæĢĐĩÄÎüļ―ÐÐéČįÏÂDD-FËųĘūĄĢ
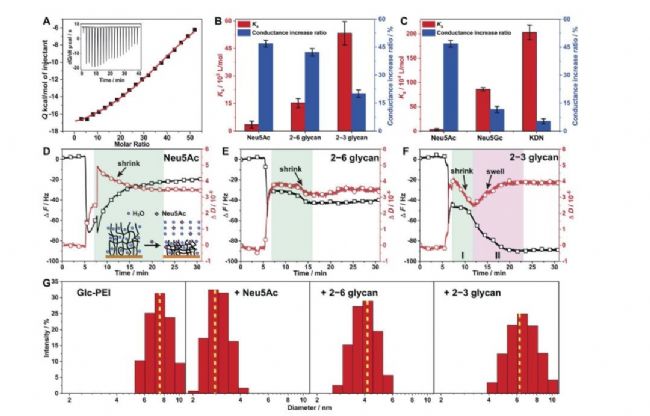
ČįÉÏDĢĻÖÐĢĐĢšD) ―ß^ŨîģõČÜŌšĮÐQ§ÖÂĩÄžąĄŨŧŊšÍÕņĘšó,îlÂĘĮúūÖðuÉÏÐÐČŧšóÆ―·ĢŽšÄÉĒĮúūÖðuÏÂÐÐĢŽēĒÓÚ15·ÖįšóÚ ÓÚÆ―·ĄĢß@ąíÃũGlc-PEIąĄÄĪ,ÔÚÎüļ―ÍŲŌšËáĖĮĢĻNeu5AcĢĐšóÖðuÃËŪ,īó·ųŋsÐĄĩ―ŌŧļüūoĩÄÏóĄĢ
(E) ģõĘžžąĄÎŧŌÆšóĢŽîlŌÆpČõĢŽēĒÁĒžīÚ ÓÚÆ―·ĢŽķøšÄÉĒÎŧŌÆŪģĢpÐĄĢŽēĒÔÚ8minČÚ ÓÚÆ―·ĢŽÕfÃũ2-6ĖĮæÔÚūÛšÏÎïÓÉÏĩÄÎüļ―ŌÔž°ūÛšÏÎïÓÃËŪʧÖØÍŽr°lÉúĄĢČŧķøĢŽÃËŪšÍĘÕŋsß^ģĖĘĮķĖšĩÄĢŽŨî―KūÛšÏÎïÓHH°lÉúÁËßmķČĩÄĘÕŋsĄĢ
(F)ĩÚIëAķÎĩÄîlŌƚ͚ÄÉĒÎŧŌÆūųpÐĄĢŽÕfÃũÔÚūÛšÏÎïÓÃËŪĘÕŋsĩÄÍŽr°lÉúÁË2-3ĖĮæĩÄÎüļ―ĄĢëSšóĢŽšÄÉĒÎŧŌÆÉÏÉýēĒÚ ÓÚÆ―ūĢŽîlŌÆÔÚĩÚķþëAķÎÏÂ―ĩēĒÚ ÓÚÆ―ūĢŽÕfÃũĒūÛšÏÎïÓÓÖ·īß^íÖðuÅōÃĄĢÕûówÉÏŋī2-3ĖĮæĩÄÎüļ―ÔėģÉÁËūÛšÏÎïÓ°lÉúÐĄ·ųķČĩÄĘÕŋsĄĢ
ąūÎÄî}ÄŋĄķBiomimetic nanochannels for the discrimination of sialylated glycans via a tug-of-war between glycan binding and polymer shrinkageĄ·ücôÔÎÄæ―ÓĢŽēéŋīÔÎÄĄĢ
°lēžÕßĢšČðĩä°ŲWÁÖŋÆžžÓÐÏÞđŦËū
ÂÏĩëÔĢš021-68370071/021-68370072
E-mailĢšvanilla.chen@biolinscientific.com
ÂÏĩëÔĢš021-68370071/021-68370072
E-mailĢšvanilla.chen@biolinscientific.com
- GardnerÉŦËĢšŌšówîÉŦyÁŋĩÄ―ĩäËĘ
- MP-SPRrzy°Đž°ûŌÔž°°Đž°ûÔÚÖēČëēÄÁÏąíÃæĩÄðĪļ―Įér
- ĘđÓÃFIDAšYßxžžÐgŌŧ·ÖįÎâķČŦ@ĩÃÓHšÍÁĶKdĩÄ·―·Ļ―é―B
- ĘđÓÃIKA ROTAVISCÐýÞDÕģķČÓyÔrĮāÓÆ·ÔÚēŧÍŽØķČÏÂĩÄÕģķČ
- ÆÏĖŅĖĮČéËá·ÖÎöxÔÚÖØ―Mĩ°°Ũé_°lž°ûÅāðBÖÐV·šŠÓÃ
- EKF ÆÏĖŅĖĮČéËá·ÖÎöxĩÄ ĒĩšÍŠÓÃ
- §áēÄÁÏĩÄCÐĩķČzyĩÄģĢÓ÷―·Ļ
- FIDAĢšĄŅŠ°YĢĻÄķū°YĢĐÔ\āĩÄÐÂÏĢÍû
- ÓĒøLovibondÔŅbßMŋÚšÄēÄīó―ĩrĢŽßīaŲĢĄ
- Gator BioÖąēĨîAļæĢš―ŌÃØAIÔOÓNovoBodyĩ°°ŨÆ―Å_
- hĮōđŦËūģÉđĶ ĒÕđĩÚķþĘŪķþīÎČŦøëŧŊWīóþ
- FIDAÉúÃüŋÆWđŦËūCEOÔLČAēĒþŌÖÐøížâWÐgC
- ÁŋĘyĘÖūīaÉúÎïĢŽžÓËŲŋįÄĪĩ°°ŨÐÂËé_°lßMģĖ
- hĮōÁÁÏāĩÚūÅÃģŽžëČÝÆũž°ëģØęPæIēÄÁÏWÐgþŨh
- ŲķũŋÆxĘÜŅûĒ ĒžÓŧļÛ°Äīóģ ^ÎïĀíWþšÏÄęþ
- ÁŋĘ&·žÖØ°õÍÆģöÐÂÆ·LeExoÍâÃÚówž{ÃŨîwÁĢ·ÖÎöx
Copyright(C) 1998-2025 ÉúÎïÆũēÄūW ëÔĢš021-64166852;13621656896 E-mailĢšinfo@bio-equip.com





