文獻解讀:MUC18靶向的PET探針研發與PDX模型可視化
封面文章
VIEW Illuminating Wellness
文獻信息
貴州大學醫學院、北京大學腫瘤醫院暨北京市腫瘤防治研究所,核醫學科,國家藥監局放射性藥物研究與評價重點實驗室,惡性腫瘤發病機制及轉化研究教育部重點實驗室等團體的研究成果Mucin 18-targeted humanized monoclonal antibody immune positron emission tomography imaging and patient-derived tumor xenograft visualization(MUC18靶向的PET探針研發與PDX模型可視化)在學術期刊《VIEW》作為封面文章(IF=9.7)發表。平生公司的小動物PET/CT(型號:Super Nova)產品在論文中提供了重要的腫瘤小鼠PET/CT圖像和定量分析。
該研究的通訊作者為北大腫瘤醫院黑色素瘤與肉瘤內科連斌主任醫師、核醫學科楊志主任、朱華研究員。
第一作者為北大腫瘤醫院與貴州大學聯合培養的博士研究張倩同學,北大腫瘤醫院杜海貞同學及馬秀利醫師。張倩,杜海貞,馬秀利,劉松,孔祥星,胡牧野,Shi Jing,Tang Yanfang,Liu Shuhui,Meng Xun,郭倩,孔燕,郭軍,連斌,楊志,朱華

文獻背景
在精確診斷各種亞型黑色素瘤的背景下,從分子角度識別具有臨床轉化潛力的生物標志物對于更全面地描述該疾病至關重要。粘蛋白18(MUC18)在主要黑色素瘤亞型的腫瘤細胞和腫瘤血管系統中高度表達,僅限于正常組織。開發了一種利用免疫正電子發射斷層掃描(PET)放射性核素偶聯藥物(RDC)和89Zr標記的人源化抗MUC18單克隆抗體(mAb)對黑色素瘤中MUC18進行無創成像的方法。對A375、Sk-Mel-28、HMVII和A549細胞以及腫瘤模型小鼠進行了研究。免疫PET用于評估免疫缺陷小鼠中三種不同的黑色素瘤細胞系衍生異種移植物(CDXs)和患者衍生腫瘤異種移植物的特異性和靶向性。開發的RDC名為89Zr-IP150,具有強大的體外穩定性和高結合親和力,可確保在人類黑色素瘤小鼠異種移植模型中對小、中、大皮下腫瘤進行可靠和特異的PET成像。值得注意的是,首次使用PDX模型成功驗證了89Zr-IP150的臨床轉化潛力。這些發現提供了一種非侵入性、實時的MUC18(+)黑色素瘤患者的早期篩查方法,對于研究MUC18靶向抗體-藥物偶聯物的早期生物學分布具有重要意義。
實驗方法
動物模型
通過將1×106細胞(懸浮在100 µL PBS中)注射入腋下,在4至5周齡雌性無胸腺裸鼠中誘導A375和HMVII腫瘤異種移植物。對于SK-Mel-28和A549細胞模型,將細胞懸浮在100 µL的PBS和Matrigel1:1混合物中,當腫瘤直徑達到<5 mm(小)、5-10 mm(中)或>10 mm(大)時,動物在植入后3周用于體內實驗。
CDX和PDX用于在體內無創地評估89Zr標記的抗MUC18抗體的特異性和靶向性。當腫瘤直徑達到5-15 mm時進行實驗。在特定時間點(注射后4、24、48、72、96、120和168小時)收集通過尾靜脈注射3.7 MBq 89Zr-IP150的模型圖像。阻斷組提前靜脈注射1毫克IP150。PET采集時間為900秒,在PET采集和重建后采集CT圖像(平生醫療科技有限公司)。PET成像原始數據被轉換為以SUV表示的色階上的假彩色最大強度投影,并通過繪制感興趣區域(ROI)獲得定量結果。
實驗結果
荷瘤鼠經尾靜脈注射約3.7 MBq 89Zr-IP150后4, 24, 48, 72, 96,120, 和168 小時進行Micro-PET/CT圖像采集,圖像結果顯示探針在不同和色素瘤模型A375,HMVII,SK-Mel-28腫瘤部位均出現明顯的放射性信號的濃聚,而在陰性模型A549腫瘤部位未觀察到明顯信號。此外,為了探究探針的臨床轉化潛力,也在更具有臨床代表性的PDX模型中進行了探針靶向性的驗證,結果表明PDX模型病灶也可以被觀察到。
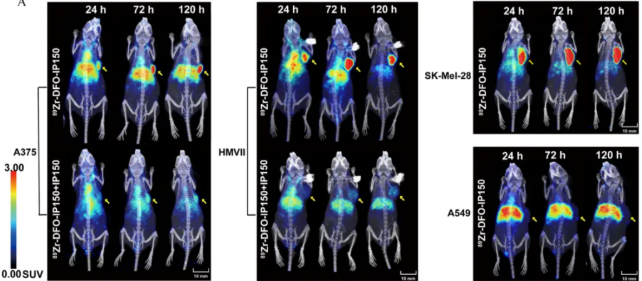
圖3(A) A375、HMVII、SK-Mel-28和A549荷瘤小鼠在尾靜脈注射89Zr-IP150后的微正電子發射斷層掃描/計算機斷層掃描(PET/CT)圖像(n=3)。
為了進一步評估89ZrIP150對黑色素瘤的特異性成像能力,使用臨床上最常用的PET成像示蹤劑18F-FDG作為對照。口服1小時后,A375和HMVII腫瘤之間的放射性濃度沒有顯著差異,18F-FDG主要積聚在心臟和腎臟等代謝器官中(圖5A)。在A375(0.96±0.06 vs.5.57±0.29)和HMVII(1.28±0.03 vs.7.11±0.08)模型中,腫瘤對18F-FDG的攝取明顯低于89Zr-IP150(p<0.001)(圖5B)。此外,18FDG的腫瘤/肌肉比率也顯著低于89Zr-IP150(A375為0.96±0.06 vs 21.48±4.40,HMVIIA為2.12±0.06 vs 21.33±3.45)(圖5C)
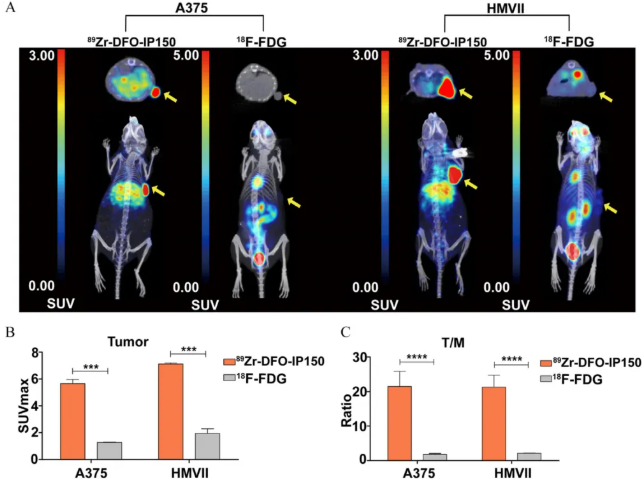
圖5(A)A375和HMVII荷瘤小鼠經尾靜脈注射89Zr-IP150或18F-氟脫氧葡萄糖(18F-FDG)后的微正電子發射斷層掃描/計算機斷層掃描(PET/CT)圖像比較(n=3/組)。(B,C)89Zr-IP150和18F-FDG的PET圖像的腫瘤攝取和T/M值,這些值表示為SUVmax(n=3)。***,p<0.001;****,p<0.0001
為了擴大本研究的臨床相關性,在MUC18(+)皮膚(圖6)和粘膜(圖S4)黑色素瘤PDX模型中評估了89Zr-IP150。在MIP和皮膚(圖6A)和粘膜(圖S4)的冠狀圖像中,從2到120小時觀察到腫瘤的顯著攝取。對于皮膚PDX模型,24小時達到最大腫瘤攝取,SUVmax為2.77±0.16,而心臟中的放射性濃度從2小時到24小時急劇下降(3.23±0.04至0.70±0.04)(圖6B)。
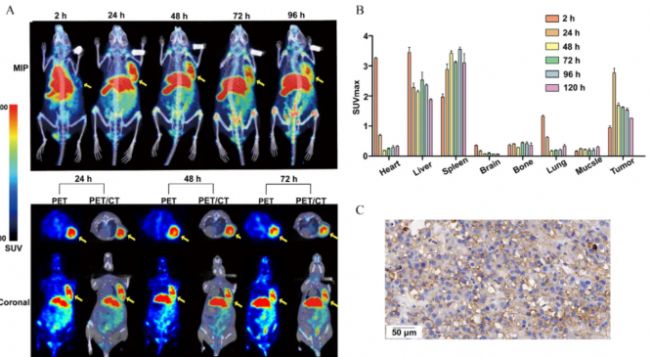
圖6(A)人類皮膚黑色素瘤患者衍生的腫瘤異種移植物(PDX)模型的MIP圖像和冠狀圖像,黃色箭頭表示腫瘤。(B)正電子發射斷層掃描(PET)圖像的感興趣區域(ROI)分析;值表示為SUVmax(n=3)。(C)PDX腫瘤中粘蛋白18(MUC18)的免疫組織化學(IHC)染色。
文獻結論
總之,本研究介紹了人源化放射性標記的MUC18特異性單克隆抗體探針的臨床前應用,該探針成功用于對各種人源化黑色素瘤小鼠模型進行成像。此外,該探針在具有臨床代表性的黑色素瘤PDX模型中顯示出有前景的腫瘤靶向作用。重要的是,成人的輻射劑量被認為相對安全,支持其未來臨床轉化的潛力。
使用設備

Super Nova® Micro PET/CT(III 代外觀圖)





