MiSelect R 在分析稀有免疫細胞免疫治療研究的應用
(一) 前言
人類 T 細胞可以靶向腫瘤特異性的突變是癌癥免疫治療的基礎, 如 Keytruda、 Opdivo這類 PD-1 靶向的藥物和 Yervoy 這類 CTLA-4 靶向的藥物,在臨床上都展示出顯著的療效。但目前對這些藥物有效的患者只占所有患者的大約 1/3,臨床都是通過 IHC 檢測腫瘤組織切片,來判斷 PD-1 等靶點的表達量,從而判斷是否適用這些藥物。而獲取腫瘤組織切片是侵入性的,很多情況下無法獲得(某些內部器官,如肝、肺等部位的組織采樣成功率很低);如果腫瘤已被切除,那么后續就無法重復取樣,也就無法進行追蹤檢測。 因此, 獲取這些對腫瘤有反應性的 T 細胞是一個挑戰。 新的研究發現從腫瘤患者的外周血里也可以分離得到腫瘤突變特異性的 T 細胞,有助于免疫治療的進一步研究【1】。
臺灣 MiCareo 公司的 MiSelect R“稀有細胞高效獲取分析系統” 是目前一款集稀有細胞(包括“循環腫瘤細胞 CTCs” 、“稀有免疫細胞”等)富集與鑒定于一體的全自動化設備,可以從腫瘤患者的外周血里檢測到對腫瘤有反應性的稀有免疫細胞,從而評估免疫治療對患者的療效, 并有助于免疫治療的進一步開展。
(二) 免疫治療研究進展
2.1 PD-1+CD8+ T 細胞是攻擊腫瘤細胞的主要族群美國 NIH 的科學家研究發現如下結論,見圖 1-5【2】。
人類 T 細胞可以靶向腫瘤特異性的突變是癌癥免疫治療的基礎, 如 Keytruda、 Opdivo這類 PD-1 靶向的藥物和 Yervoy 這類 CTLA-4 靶向的藥物,在臨床上都展示出顯著的療效。但目前對這些藥物有效的患者只占所有患者的大約 1/3,臨床都是通過 IHC 檢測腫瘤組織切片,來判斷 PD-1 等靶點的表達量,從而判斷是否適用這些藥物。而獲取腫瘤組織切片是侵入性的,很多情況下無法獲得(某些內部器官,如肝、肺等部位的組織采樣成功率很低);如果腫瘤已被切除,那么后續就無法重復取樣,也就無法進行追蹤檢測。 因此, 獲取這些對腫瘤有反應性的 T 細胞是一個挑戰。 新的研究發現從腫瘤患者的外周血里也可以分離得到腫瘤突變特異性的 T 細胞,有助于免疫治療的進一步研究【1】。
臺灣 MiCareo 公司的 MiSelect R“稀有細胞高效獲取分析系統” 是目前一款集稀有細胞(包括“循環腫瘤細胞 CTCs” 、“稀有免疫細胞”等)富集與鑒定于一體的全自動化設備,可以從腫瘤患者的外周血里檢測到對腫瘤有反應性的稀有免疫細胞,從而評估免疫治療對患者的療效, 并有助于免疫治療的進一步開展。
(二) 免疫治療研究進展
2.1 PD-1+CD8+ T 細胞是攻擊腫瘤細胞的主要族群美國 NIH 的科學家研究發現如下結論,見圖 1-5【2】。
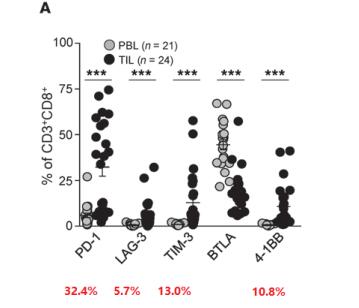
圖 1. 對于攻擊腫瘤細胞的 CD8+ TILs 細胞, PD-1+是表達多的族群(32.4%),其次是
TIM-3+(13.0%)、 4-1BB+(10.8%)、 LAG-3+(5.7%)【2】。
TIM-3+(13.0%)、 4-1BB+(10.8%)、 LAG-3+(5.7%)【2】。
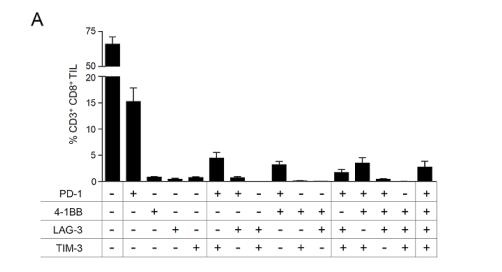
圖 2. PD-1 和其他 4-1BB、 LAG-3、 TIM-3 受體在 CD8+ TILs 細胞中有共表達性,顯然 PD-
1+是主要的族群【2】。
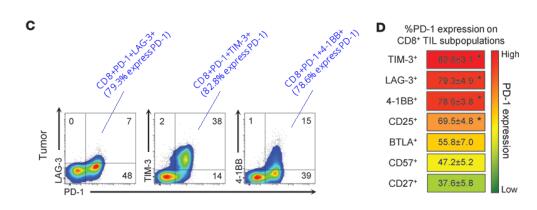
圖 3. 在新鮮腫瘤組織中, TIM-3+、 LAG-3+、 4-1BB+的細胞,大多數表現出 PD-1+,如
82.8%的 TIM-3+表達 PD-1、 79.3%的 LAG-3+表達 PD-1、 78.6%的 4-1BB+表達 PD-1,說明
PD-1+仍然是主要的族群【2】。
1+是主要的族群【2】。

圖 3. 在新鮮腫瘤組織中, TIM-3+、 LAG-3+、 4-1BB+的細胞,大多數表現出 PD-1+,如
82.8%的 TIM-3+表達 PD-1、 79.3%的 LAG-3+表達 PD-1、 78.6%的 4-1BB+表達 PD-1,說明
PD-1+仍然是主要的族群【2】。
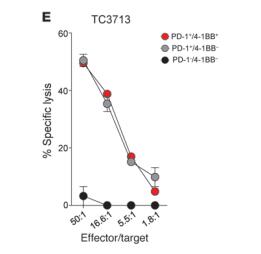
圖 4. 不管 4-1BB 是陰性還是陽性, 只要 PD-1 陽性, 有 PD-1+的 TILs 細胞在和腫瘤細胞系
共培養時,對腫瘤細胞就有溶菌作用【2】。
共培養時,對腫瘤細胞就有溶菌作用【2】。
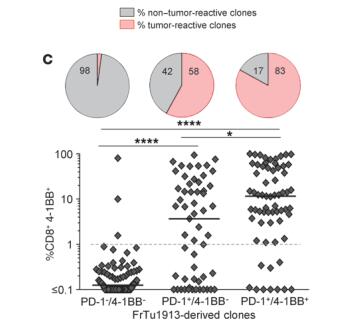
圖 5. PD-1 的表達決定了對腫瘤有反應的 CD8+ TILs 細胞的數目:對 PD-1+/4-1BB+的 CD8+TILs 細胞,對腫瘤有反應的百分比高,其次是 PD-1+/4-1BB-的 CD8+ TILs 細胞,反應比例小的是 PD-1-/4-1BB-的 CD8+ TILs 細胞【2】。
2.2 PD-1+CD8+ T 細胞比例高的人,對免疫治療反應較好對非小細胞肺癌患者,用 PD-1 免疫阻斷劑治療時, PD-1+CD8+細胞比例高的人,對免疫治療反應較好【3】,見圖 6-7。
2.2 PD-1+CD8+ T 細胞比例高的人,對免疫治療反應較好對非小細胞肺癌患者,用 PD-1 免疫阻斷劑治療時, PD-1+CD8+細胞比例高的人,對免疫治療反應較好【3】,見圖 6-7。
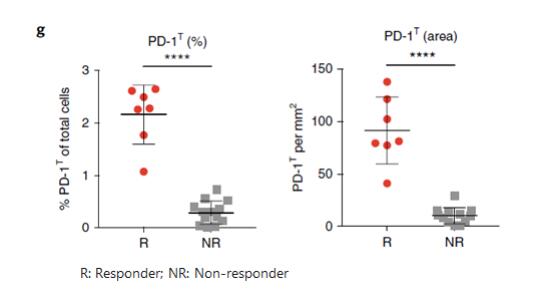
圖 6.對于免疫治療有反應的患者, PD-1T (高表達) TILs 細胞在所有細胞中的比例和單位面積的數量均高于沒有反應的患者【3】。
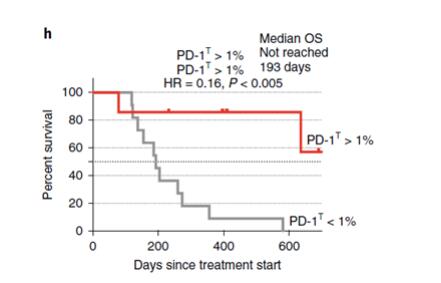
圖 7. PD-1T (高表達) TILs 細胞>1%的患者,總體生存率(OS)要高于<1%的患者【3】。
2.3 液體活檢研究稀有免疫細胞
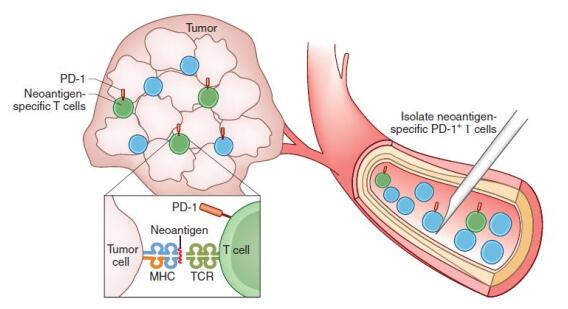
以往 TILs 的分離僅能從腫瘤組織中獲取,但組織切片的獲取具有很多不便性及侵入性。現在, 與腫瘤組織內部的 TILs 細胞一樣,在患者的外周血里也能發現與 TILs 一致的 PD-1+CD8+的 T 細胞(圖 8)。 腫瘤細胞的刺激使淋巴系統產生大量的功能性免疫細胞,再運送到腫瘤組織周圍,所以在外周血中就可以獲取與 TILs 一致的免疫細胞。 研究外周血循環中的 CD8+ T 細胞上的 PD-1 表達,為研究腫瘤組織內部的抗腫瘤 T 細胞提供了一扇窗戶,也成為進行免疫治療的標志物, 有助于分離出對腫瘤有反應的 CD8+ T 細胞,進行免疫治療【1】。
2.3 液體活檢研究稀有免疫細胞
以往 TILs 的分離僅能從腫瘤組織中獲取,但組織切片的獲取具有很多不便性及侵入性。現在, 與腫瘤組織內部的 TILs 細胞一樣,在患者的外周血里也能發現與 TILs 一致的 PD-1+CD8+的 T 細胞(圖 8)。 腫瘤細胞的刺激使淋巴系統產生大量的功能性免疫細胞,再運送到腫瘤組織周圍,所以在外周血中就可以獲取與 TILs 一致的免疫細胞。 研究外周血循環中的 CD8+ T 細胞上的 PD-1 表達,為研究腫瘤組織內部的抗腫瘤 T 細胞提供了一扇窗戶,也成為進行免疫治療的標志物, 有助于分離出對腫瘤有反應的 CD8+ T 細胞,進行免疫治療【1】。

圖 8.外周血循環中可以分離出新抗原特異性的 PD-1+ T 細胞【1】。
2.4 流式細胞儀很難檢測到外周血中的稀有免疫細胞
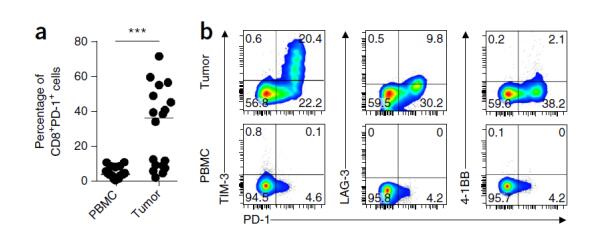
圖 9. 在黑色素瘤患者的外周血中,也能發現新抗原特異性的淋巴細胞。與腫瘤組織內部
相比,外周血(PBMC)中的 PD-1+CD8+的 T 細胞數量非常少,流式細胞儀幾乎無法檢測到【4】。
(三) MiSelect R 檢測稀有免疫細胞
3.1 MiSelect R 的高靈敏度
由于 MiSelect R 的創新性設計, 其對稀有細胞的捕獲和鑒定具有高特異性和高靈敏度, 對于細胞數很稀少的族群 (<100 cells/mL) , 流式細胞儀已經無法檢測到,而MiSelect R 可以檢測(圖 10)【5】。 因此可以用 MiSelect R 來檢測極微量的外周血中的稀有免疫細胞。
(三) MiSelect R 檢測稀有免疫細胞
3.1 MiSelect R 的高靈敏度
由于 MiSelect R 的創新性設計, 其對稀有細胞的捕獲和鑒定具有高特異性和高靈敏度, 對于細胞數很稀少的族群 (<100 cells/mL) , 流式細胞儀已經無法檢測到,而MiSelect R 可以檢測(圖 10)【5】。 因此可以用 MiSelect R 來檢測極微量的外周血中的稀有免疫細胞。
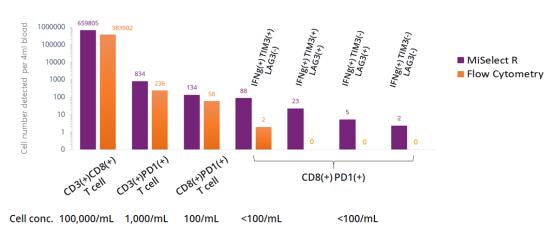
圖 10. 對于細胞數很稀少的族群 (<100 cells/mL) , 流式細胞儀已經無法檢測到,而MiSelect R 可以檢測到; 而對于>100 cells/mL 的族群, MiSelect R 檢測到的細胞數量,幾乎是流式的 2 倍以上,說明 MiSelect R 的靈敏度比流式更高【5】。
3.2 外周血稀有免疫細胞數量對療效的影響
科學家研究了“肝細胞癌”和“腎細胞癌”的 anti-PD1(Keytruda) 免疫治療, 對 36名“肝細胞癌”患者和 10 名“腎細胞癌”患者, 在免疫治療之前抽取患者的外周血, 用MiSelect R 檢測稀有免疫細胞的數量。實驗結果表明: 外周血里稀有 PD-1+CD8+ T 細胞和PD1+CD4+ T 細胞數目多的患者,其總生存率(OS)和無進展生存率(PFS)均明顯高于此類稀有 T 細胞數目少的患者(圖 11-13)【5】。
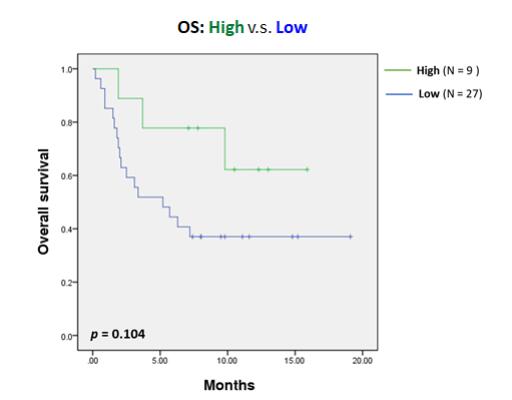
圖 11.肝細胞癌患者的外周血稀有 PD-1+CD8+ T 細胞(攻擊性 T 細胞) 數目與 OS 的關系【5】。
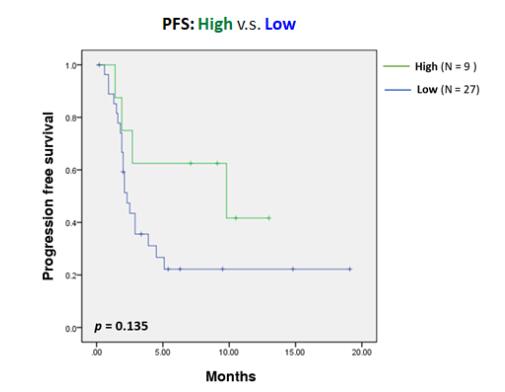
圖 12.肝細胞癌的外周血稀有 PD-1+CD8+ T 細胞(攻擊性 T 細胞) 數目與 PFS 的關系【 5】。
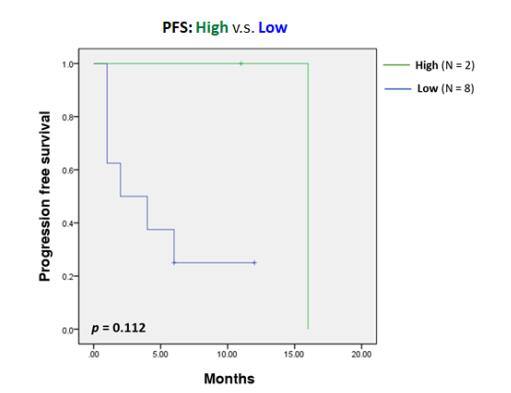
圖 13. 腎細胞癌的外周血稀有 PD-1+CD4+ T 細胞(調節性 T 細胞) 數目與 PFS 的關系【 5】。
3.3 其他免疫檢查點抑制劑的研究
目前針對免疫檢查點抑制劑的臨床研究的統計結果如圖 14,可見有部分研究是針對稀有的免疫檢查靶點的,如 TIM-3、 LAG-3、 VISTA、 KIR, 因為 MiSelect R 是通過抗體來標記免疫細胞上的 marker, 所以 MiSelect R 均可有助于此類實驗的開展【6】。
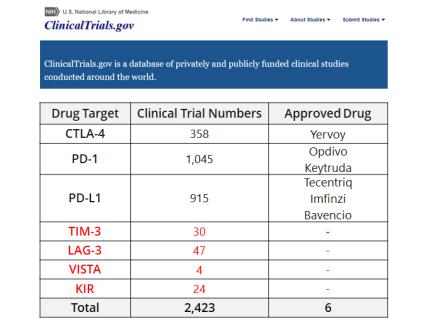
圖 14. 免疫檢查點抑制劑的臨床研究的統計結果【6】。
3.4 MiSelect R 檢測稀有免疫細胞的影像
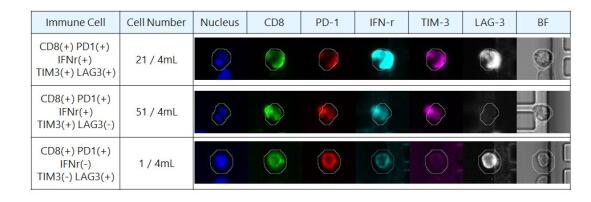
圖 15. MiSelect R 檢測結直腸癌患者的稀有免疫細胞的影像,可見可以針對 IFN-r、 TIM-
3、 LAG-3 靶點進行標記【5】。
(四) MiSelect R 介紹
臺灣 MiCareo 公司的 MiSelect R“稀有細胞高效獲取分析系統” 是目前一款集稀有細胞(包括“循環腫瘤細胞 CTCs” 、“稀有免疫細胞”等)富集與鑒定于一體的全自動化設備,技術法寶包括微流控技術、激光分選、體積過濾和熒光標記成像,既可以對稀有細胞進行計數、分析和鑒定(生物標志物分析),又可以獲得高捕獲率、高純度、高活性的稀有細胞,供下游研究使用。
MiSelect R 的原理見: 稀有細胞檢測的突破——MiSelect R 助力稀有免疫細胞檢測。

圖 16. Miselect R 稀有細胞高效獲取分析系統,全自動,省時省力。
(五) 總結
和市面上其他稀有細胞檢測方法不同, MiSelect R 可對稀有細胞進行計數、分析、鑒定,并獲得活細胞。具有高純度(>60%) 、高捕獲率(98.5%) 、高細胞活性(>99%) 、 高檢測靈敏度、 可重復性(CV<10%) 、可視性、 廣譜性以及全自動運行(操作簡單,全血上樣,全自動運行,單機集成)等優點,可檢測 EpCAM 低表達的腫瘤細胞株,靈敏度是流式細胞儀的 2 倍。可用于 CTCs 研究、癌癥藥物的伴隨診斷、稀有功能性免疫細胞研究,或產前無創檢測,是非常強大的稀有細胞高效獲取分析系統。
更多資訊,請聯系:森西科技有限公司,電話: 010-61666616,熱線: 400-687-6366,
郵箱: info@sinsitech.com,網址: www.sinsitech.com。掃描以下二維碼,關注微信公眾
號:

參考文獻:
【1】 Schumacher,T.N.& Scheper,W., A liquid biopsy for cancer immunotherapy,
Nature Medicine, Volume22, No.4, 2016, pp.340-341.
【2】 Gros,G.,et al., PD-1 identifies the patient-specific CD8+ tumor-reactive
repertoire infiltrating human tumors, The Journal of Clinical
Investigation, Volume124, No.5, 2014, pp.2246-2259.
【3】 Thommen,D.S.,et al., A transcriptionally and functionally distinct PD-1+
CD8+ T cell pool with predictive potential in non-small-cell lung cancer
treated with PD-1 blockade, Nature Medicine,
https://doi.org/10.1038/s41591-018-0057-z.
【4】 Gros,A.et.al., Prospective identification of neoantigen-specific
lymphocytes in the peripheral blood of melanoma patients, Nature
Medicine, published online 22 February 2016.
【5】 MiCareo Clinical Project Documents.
【6】 Website: ClinicalTrials.gov
【1】 Schumacher,T.N.& Scheper,W., A liquid biopsy for cancer immunotherapy,
Nature Medicine, Volume22, No.4, 2016, pp.340-341.
【2】 Gros,G.,et al., PD-1 identifies the patient-specific CD8+ tumor-reactive
repertoire infiltrating human tumors, The Journal of Clinical
Investigation, Volume124, No.5, 2014, pp.2246-2259.
【3】 Thommen,D.S.,et al., A transcriptionally and functionally distinct PD-1+
CD8+ T cell pool with predictive potential in non-small-cell lung cancer
treated with PD-1 blockade, Nature Medicine,
https://doi.org/10.1038/s41591-018-0057-z.
【4】 Gros,A.et.al., Prospective identification of neoantigen-specific
lymphocytes in the peripheral blood of melanoma patients, Nature
Medicine, published online 22 February 2016.
【5】 MiCareo Clinical Project Documents.
【6】 Website: ClinicalTrials.gov
標簽:
稀有細胞.免疫治療
Copyright(C) 1998-2025 生物器材網 電話:021-64166852;13621656896 E-mail:info@bio-equip.com





