Naica數字PCR在湖南疾控檢測精子、全血、尿糞樣本中新冠病毒的應用
Paper -1:
全球新型冠狀病毒肺炎疫情日益嚴峻,除了齊心協力對抗病毒外,科研人員也在對新冠病毒進行更深入的研究,比如疫苗研發,感染后患者生理機能是否會受影響等。其中,關于新冠對生殖方面的影響一直備受關注,迄今為止,已在精液和精子中檢測到27種病毒。那么在新冠大流行的背景下,SARS-CoV-2(covid-19)是否存在于精液中呢?如果精液樣本中存在極低病毒載量的SARS-CoV-2(covid-19),一旦被使用,那么必定會有傳染風險。
湖南省疾病預防控制中心以湖南省人類精子庫在大流行期間和之后收集的冷凍精液為研究對象,開展了一項回顧性研究,并發表在《Reproductive BioMedicine Online》雜志上。 研究包括來自100個供體的100對精液和血液樣本,考慮到兩種標本的病毒載量均較低,所以研究人員使用了自主改良的一步法-單管巢式定量PCR(OSN-qRT-PCR)進行SARS-CoV-2(covid-19)檢測。此外,為了避免出現“假陰性結果”,使用Naica™數字PCR(cd-PCR)對來自陰性精液樣品的RNA進行了第二輪群體檢測。

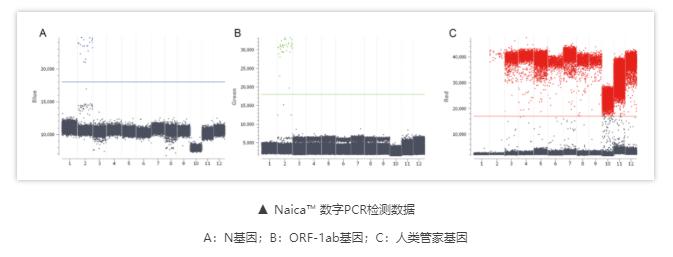
結果:對于單個血液和精液樣本,分別檢測了核衣殼蛋白(N)和開放閱讀框(ORF-1ab)基因,在100對樣本中均呈陰性。此外,根據cd-PCR結果,群體檢測的RNA樣本中,每孔均> 20,000個微滴,并且均不存在陽性液滴。
結論:冠狀病毒大流行期間和之后,湖南省人類精子庫冷凍保存的精液均不含SARS-CoV-2(covid-19),可以安全使用。
Paper -2:
本研究對已經確診的3例新型冠狀病毒肺炎患者按照不同時間的全血、尿液、糞便標本同時進行qPCR和Naica™數字PCR(cd-PCR)的核酸檢測,并比較了兩種方法檢測各類樣本中2019-nCoV的差異性,提出改進2019-nCoV核酸檢測的綜合策略,為核酸檢測陰性患者提供更多診斷支持。
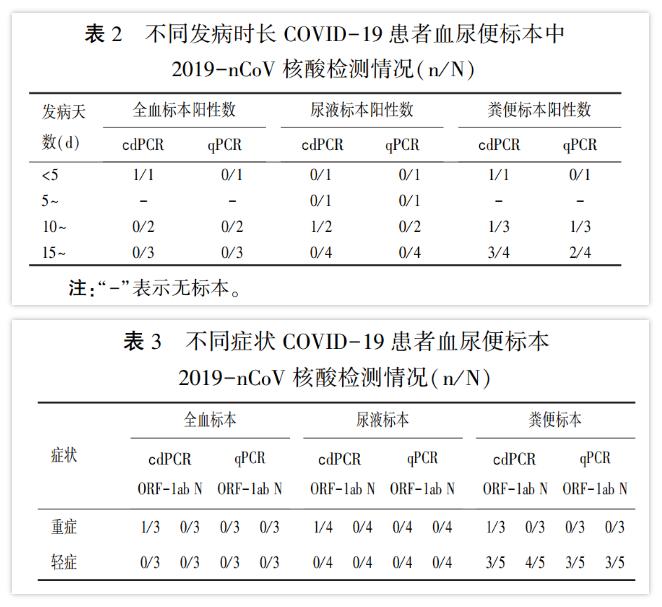
本實驗中數字PCR在病例發病早、中、晚期標本中均能檢測到陽性微滴,而qPCR漏檢了發病小于5天的標本,檢測到的陽性核酸均以中晚期為主。(表2)這也解釋了受檢測方法靈敏度的局限性,目前大部分假陰性患者都處于疾病發展的早期。此外,在本次實驗中數字PCR在重癥病例的三種標本中均測到陽性微滴,但因為血、尿和可疑糞便的標本病毒載量偏低,qPCR檢測均為陰性。(表3)
總之,數字PCR技術可以有效克服qPCR靈敏度不足的難題,精準捕捉到病毒載量較低的血液、尿液和可疑的糞便或肛拭子標本,是qPCR的有益補充,為幫助臨床醫生準確判斷早期感染及患者是否真正痊愈起到了積極的作用,對2019-nCoV的長期監控有重要的意義。
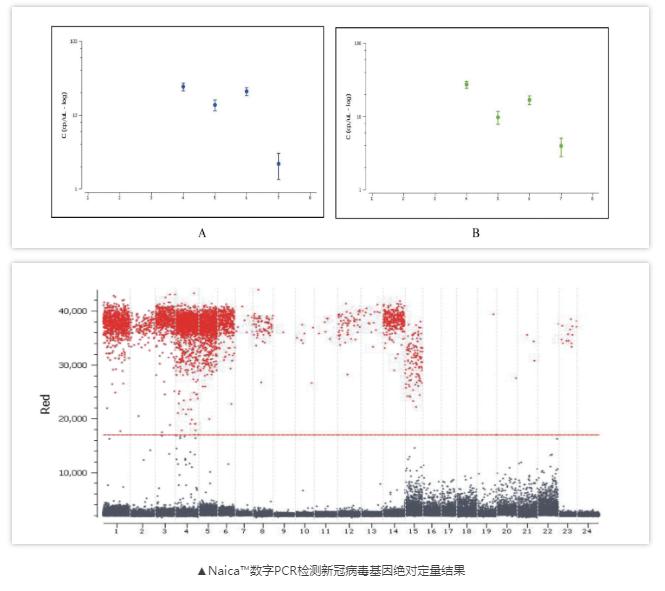
兩篇Paper均采用了--Naica™數字PCR平臺

法國Stilla Technologies公司的Naica™數字PCR技術在進行核酸檢測時具有獨特的優勢。系統利用cutting-edge微流體創新型芯片—Sapphire芯片作為數字PCR過程的耗材。樣品通過毛細通道網格以30,000個微滴的形式進入2D芯片中。3色熒光檢測儀器,整個流程只需要2.5小時,并可進行數據的質控和結果追溯分析,獲得的數據真實可靠。
操作流程:

原文鏈接:
Paper1:doi.org/10.1016/j.rbmo.2020.11.015
Paper2:doi:10.3969/j.issn.1006-3110.2020.11.009





