激光共聚焦顯微鏡助力腫瘤抑制劑研究

01 文章內容
文章聚焦于鐵死亡抑制蛋白FSP1(ferroptosis suppressor protein-1)的研究。研究人員通過篩選小分子庫發現icFSP1這一新型 FSP1 抑制劑,它能誘導鐵死亡,且作用機制不同于以往的iFSP1,不直接抑制FSP1酶活性,而是使FSP1發生亞細胞重定位并凝聚,進而促進FSP1相分離,引發脂質過氧化和鐵死亡。這一過程依賴FSP1的N端肉豆蔻酰化、特定氨基酸殘基及相關結構區域。體內實驗顯示icFSP1能抑制腫瘤生長,通過誘導FSP1從膜上解離和相分離形成凝聚物,引發脂質過氧化和鐵死亡。文章中利用激光共聚焦顯微鏡為探究icFSP1誘導鐵死亡機制提供關鍵依據:
1.icFSP1對hFSP1亞細胞定位的影響:
展示了對穩定過表達FSP1–EGFP–Strep的野生型細胞用2.5μM的icFSP1處理后立即采集的代表性時間推移熒光圖像1(下圖c)。結果顯示,icFSP1處理后,細胞出現明顯焦點和凝聚物,而iFSP1處理組無此現象,表明icFSP1顯著改變hFSP1亞細胞定位,此變化先于脂質過氧化和鐵死亡。
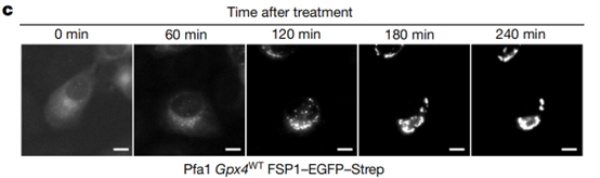
2.FSP1凝聚物形成過程及特性:
對穩定過表達hFSP1-EGFP-Strep的Pfa1細胞用 icFSP1處理,在不同時間點拍攝熒光圖像2(下圖d),觀察到凝聚物數量隨時間增加,體現其形成的時間依賴性。用鐵死亡標記物(Liperfluo)與碘化丙啶(PI)對穩定過表達hFSP1-BFP的細胞進行共染色處理,標記脂質過氧化和細胞死亡情況(下圖e)。碘化丙啶具有特殊的染色特性,只有當細胞膜出現破損,其才能進入細胞并對細胞核進行染色。使用icFSP1處理表達hFSP1-BFP的細胞后,細胞內迅速誘導產生凝聚物。緊接著,Liperfluo發生氧化,這意味著細胞內脂質過氧化反應開始啟動。此后,細胞內的脂質過氧化物信號持續增強,直至細胞對碘化丙啶染色呈現陽性,這一現象表明細胞膜已破裂,細胞走向死亡。從整個過程可以清晰地看到,FSP1亞細胞定位的改變發生在脂質過氧化和鐵死亡之前,這一結果為深入理解鐵死亡的發生機制提供了重要線索。
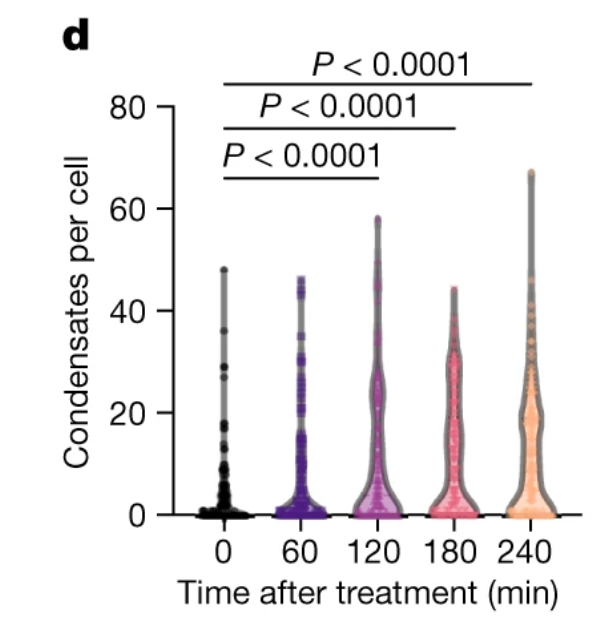
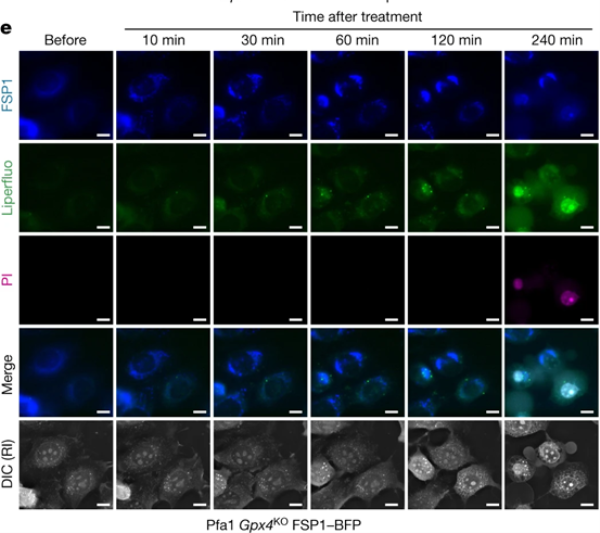
> Tip1,2:
中心(公司)超高分辨率激光共聚焦顯微鏡平臺,提供配套細胞培養箱,可以供即時或不同時間點采集圖像的實驗,可確保實驗的時效性。
3.FSP1凝聚物的動態變化及相分離特性:
觀察穩定過表達hFSP1-EGFP-Strep的Pfa1細胞,發現icFSP1處理后凝聚物動態自由移動并融合(下圖a),洗脫抑制劑后凝聚物變化可逆(下圖b)。進行熒光漂白恢復(FRAP)分析3(下圖 c、d),發現早期凝聚物有FRAP現象,晚期無,結合其類似液滴的特性,表明hFSP1凝聚物可能涉及相分離。
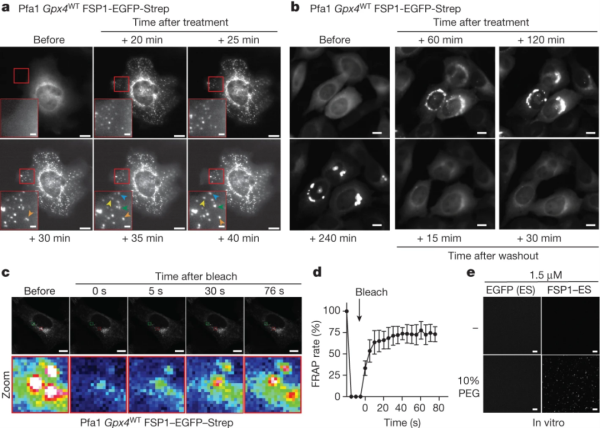
> Tip3:
中心(公司)超高分辨率激光共聚焦顯微鏡平臺配備有熒光漂白恢復(FRAP)功能,可進行樣本定點光照射,并提供光漂白恢復實驗數據(時長、圖像等)。
4.FSP1凝聚物與亞細胞結構的關系:
對穩定過表達hFSP1-EGFP-Strep的細胞用icFSP1處理后,與多種細胞器特異性標記物共染4(下圖b),結果顯示hFSP1凝聚物不與內質網、高爾基體、脂質滴、內體、溶酶體等細胞器共定位,表明其并非定位于特定細胞器。
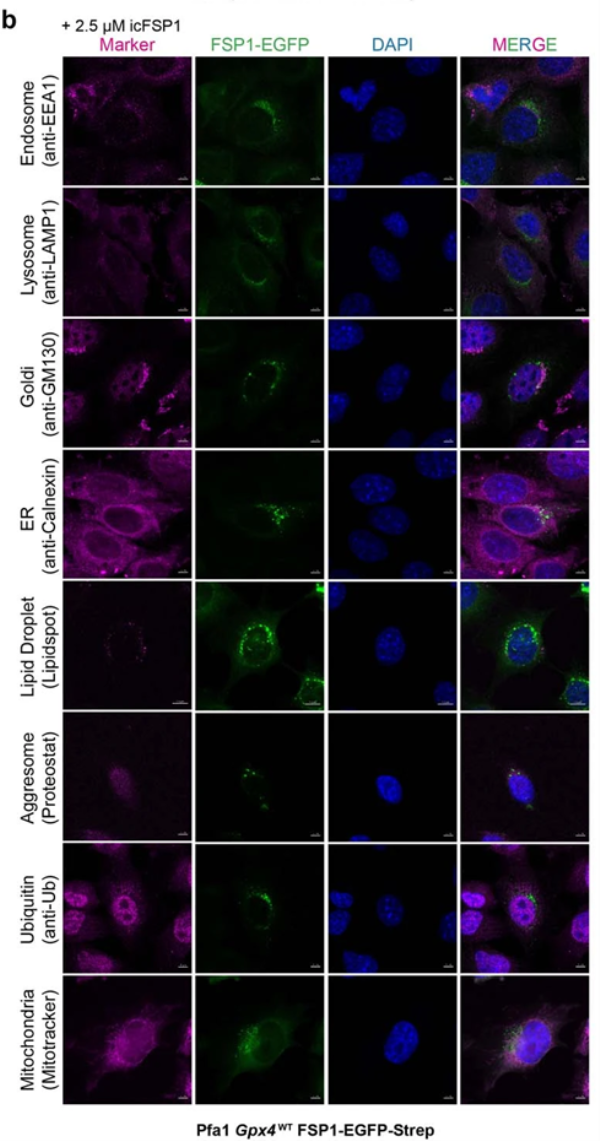
> Tip4:
中心(公司)超高分辨率激光共聚焦顯微鏡平臺可進行多通道(410-850nm)同時成像,同時提供單通道和多通道合并數據,多通道樣本可根據客戶要求提供個性化通道合并數據。
5.體內實驗中FSP1凝聚物檢測:
對腫瘤組織進行免疫熒光染色,用抗HA(hFSP1)抗體標記(下圖g、h),在icFSP1處理的腫瘤組織中,觀察到hFSP1凝聚物信號增強,表明icFSP1在體內可誘導FSP1相分離,促進脂質過氧化。對過表達不同FSP1突變體的腫瘤組織染色(下圖h),發現Q319K突變體在icFSP1處理后無凝聚物,細胞對icFSP1耐藥,驗證特定氨基酸殘基在FSP1相分離和藥物敏感性中的重要性。
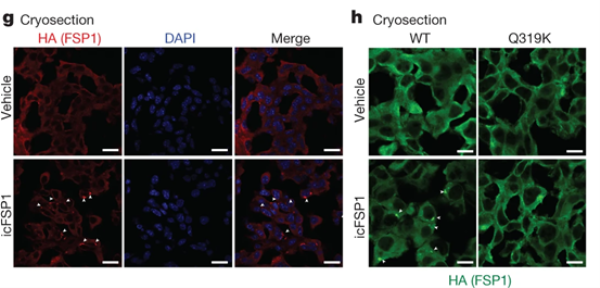
02 文章總結
該研究揭示了icFSP1獨特的作用機制,即通過誘導FSP1從膜上解離和相分離形成凝聚物,引發脂質過氧化和鐵死亡。這為理解FSP1的調控機制提供了新視角,也為開發新型抗癌療法提供了潛在的藥物靶點和理論依據,未來應進一步開發同時靶向cyst(e)ine–GSH–GPX4節點和FSP1系統的藥物,以更有觸發腫瘤細胞鐵死亡,為攻克癌癥這一醫學難題帶來新的曙光。
03 平臺介紹
中心(公司)超高分辨率激光共聚焦顯微鏡平臺搭建的Leica Stellaris 5超高分辨率激光共聚焦系統,具有22mm均勻大視場及8K超高清掃描分辨率兩大優勢,同時搭載Power HyD檢測器,可實現更高的光子探測效率。整合的多層智能模塊體系,包含精準自聚焦、全景拼圖、多維時序成像以及光譜解碼等功能組件,尤其配備專業級共定位分析與智能三維重構系統,通過模組化擴展設計持續賦能生命科學探索新邊界。






