Exactive Plus EMR ¸ßˇÖąæŲ|×VxŦFˇĮ×ĐÔ îBADCs ËÎīĩġÖÎö
Āîėo
ŲÄŦīwĘĀ ŋÆŧŧŖ¨ÖĐøŖŠĶĐĪŪšĢËžÉĢ×VŲ|×V˛ŋ
îĘįžũ ínÄîēÍ Ë]Áĸ
ÉĪēŖĐÂĀíÄîÉúÎīátËŋÆŧŧĶĐĪŪšĢËž
ęPæIÔ~
Exactive Plus EMRŖģADCsŖģcysteine -linked ADCsŖģNative MS
1 Į°ŅÔ
ÎŋËÂĄŋšķwąģÕJéĘĮžßĶиßļČĖØŽĐÔĩÄ°ĐĪōËÎīŖŦÆäĻÄ[Áöŧ°ûĩÄ°ĐĪōĐÔˇĮŗŖ¸ßĄŖļøŋšķw- ËÎīÅŧÂÎīŖ¨Antibody-drug conjugatesŖŦŌÔĪÂēˇQADCsŖŠŧŧĐgŖŦžÍĘĮÔÚŋšķwĩ°°×ĩÄĖØļ¨°ąģųËáÉĪÅŧžßĶĐŋšÄ[Áö×÷ĶÃĩĸßЧĒģ¯¯ËÎīŖ¨ģōˇQĐĄˇÖ×ĶËÎīŖŠŖŦŌÔÔöŧĶÎŋËÂĄŋšķwĩÄ¯Đ§Ąĸ˛ĸŊĩĩÍĐĄˇÖ×ĶËÎīĩÄļžĐÔĄŖĪāąČÎŋËÂĄŋšķwŖŦADCs ËÎīĩÄÉúŽaš¤Ë¸üéÍësŖŦŌō´ËéÁËąŖ×CADCs ËÎīĩÄ°˛ČĢĐÔēÍĶĐЧĐÔŖŦĐčĻADCs ËÎīĩÄŲ|ÁŋßMĐĐąOŋØĄŖËÎīŋšķwąČŖ¨drug to antibody ratioŖŦŌÔĪÂēˇQDARŖŠĘĮÔurADCs ËÎīĩÄÉúŽaš¤ËēÍŽaÆˇŲ|ÁŋĩÄŌģÖØŌĒ
ĸĩĄŖÄŋĮ°´ķ˛ŋˇÖÉĪĘĐēÍÔÚŅĐADCs ËÎīÖ÷ŌĒ°üĀ¨ģųĶÚŋšķw×ÔÉíĩÄŲ°ąËáßMĐĐÅŧÂĩÄADCs ËÎīŖ¨lysine-linked ADCsŖŠēÍģųĶÚŋšķw×ÔÉíæégļūÁōæIŊßÔēķĩÄ°ëë×°ąËáßMĐĐÅŧÂĩÄADCs ËÎīŖ¨cysteine -linked ADCsŖŠŖ¨D1ŖŠĄŖÉîADCs ĩÄDAR yļ¨Í¨ŗŖĶĐUVĄĸHICēÍMSČũˇNˇŊˇ¨ŖŦÆäÖĐMSzyˇŊˇ¨ŌōÆäŋėËŲĄĸė`ÃôļȸßēÍ´ķĩÄļ¨ĐÔšĻÄÜĩČücŖŦĶúíĶúVˇēĩØąģĶÃĶÚyļ¨ADCs ĩÄDARĄŖÄŋĮ°MS ĶÃĶÚyļ¨ADCs ĩÄDAR ͨŗŖĘĮģųĶÚ÷ŊyĩÄRPLC/MS ÆŊÅ_ŖŦÔÆŊÅ_ĪÂRPLC ˛ÉĶÃĩÄÁ÷ĶĪāŗĘËáĐÔŖŦĮŌēŦĶĐŨ^¸ßâļČĩÄŌŌëæŖŦĩ°°×ÔÚ´ËlŧūĪ´ķļā°lÉú×ĐÔŖŦ Ōō´Ëyļ¨ŊYšûĀ¸ņŌâÁxÉĪÖvˇ´ĶŗĩÄĘĮADCs ×ĐÔēķĩÄDARĄŖĻĶÚlysine-linked ADCs ļøŅÔŖŦÉĪĘö×ĐÔlŧū˛ģĶ°íÆäŋšķwŊYĩÄÍęÕûĐÔŖŦšĘRPLC/MS ÆŊÅ_˛ģĶ°íÆäDAR yļ¨ĄŖČģļøŖŦ ĻĶÚcysteine-linked ADCs ļøŅÔŖŦÉĪĘö×ĐÔlŧūÆÆÄÁËžSŗÖŋšķwŋÕégŊYĩġĮš˛r×÷ĶÃŖŦADCs ˛ŋˇÖŊâëxÆäŨpæģōÖØæŖŦšĘRPLC/MS ÆŊÅ_oˇ¨ĶÃĶÚÆäDAR yļ¨ĄŖëSÖøˇĮ×ĐÔŲ|×VŖ¨Native MSŖŠŧŧĐgĩIJģā°lÕšēÍÍÆVŖŦ˛ÉĶÃˇĮ×ĐÔŲ|×VßMĐĐcysteine-linked ADCs ˇÖÎöī@ĘžÁË´ķĩÄĒĶÃÁĻĄŖ
Thermo ScientificTM ExactiveTM Plus EMR Ų|×VxąŖŗÖÁËOrbitrap ¸ßˇÖąæÂĘĄĸ¸ßŲ|ÁŋžĢļČĩÄŨŖŦÍŦrUÕšŲ|ÁŋĩˇļúÖÁm/z 20000ŖŦ˛ĸĮŌÔÚĶ˛ŧūÔOĶÉĪĖáÉũ¸ßŲ|ÁŋļËëx×ĶĩÄ÷ŨЧÂĘŖŦ¸ÄßMÁËHCD ēÁĻŖŦĘšÆä¸üŧĶßmĶÃĶÚÍęÕûĩ°°×Ų|ĩġÖÎöĄŖ
ßmĶÃĶÚąŖÁôĶĐČũŧēÍËÄŧŊYĩġĮ×ĐÔĩ°°×Ų|ēÍĩ°°×ÍēĪÎīĩÄŊYWĄĸÍØäWŅĐžŋŌÔŧ°ÉúÎīÖÆËÖСĮ×ĐÔ îBĪÂcysteine-linked ADCs ĩġÖÎöĄŖ
ąžōŊ¨ÁĸÁËģųĶÚExactiveTM Plus EMR ēÍProtein Deconvolution 3.0 ÜŧūĩġĮ×ĐÔ îBĪÂĩ°°×Ų|ĩġÖÎöÁ÷ŗĖŖ¨D2ŖŠŖŦ˛ĸŗÉšĻĶÃĶÚcysteine-linked ADCs ĩġÖÎöŖŦyļ¨ŨdĶвģÍŦËÎīˇÖ×ĶĩĩÄADCsģėēĪÎīĩÄžĢ´_ˇÖ×ĶÁŋŖŦ˛ĸyļ¨ÆäDARÖĩĄŖ
D1 Cysteine-linked ADCs ĘžŌâD
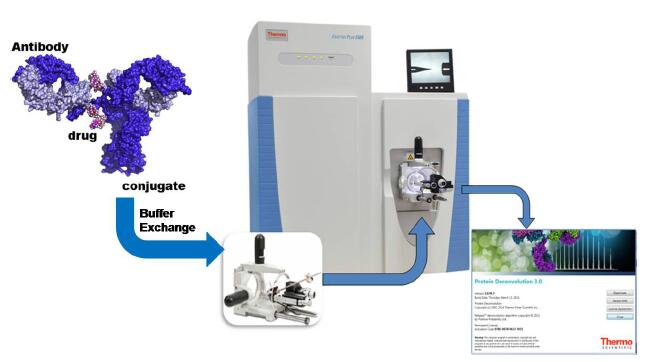
D2 ˇĮ×ĐÔ îBCysteine-linked ADCs ĩġÖÎöÁ÷ŗĖ
2ōlŧū
2.1˛ÄÁĪÅcˇŊˇ¨
ĶÆˇPCTéCysteine-linked ADCsŖŦPNGase FČĨĖĮģųģ¯ēķŖŦ˛ÉĶÃMicro Bio-Spin® Chromatography ColumnsßMĐĐž_ČÜŌēŊģQŖŦąŖ´æĶÚ100 mM ŌŌËáä@Ŗ¨pH 7.0ŖŠÖĐŖŦÅäÖÆŗÉâļČé5.5 ĻĖMĩÄČÜŌēäĶÃĄŖ
2.2Ų|×VˇÖÎö
|
Ų|×Vx |
Thermo Scientific Exactive Plus EMR |
|
ëx×ĶÔ´ |
NanoFlex Source with emitter |
|
Ų|×Vĩū˛Éŧ¯ÄŖĘŊ |
Direct Infusion |
|
ëx×ĶÄŖĘŊ |
Õũëx×Ķ |
|
ėFëē |
1.8 KV |
|
ÃĢŧšÜØļČ |
275 Ąæ |
|
ÃĢŧšÜØļČ |
ON |
|
Ų|Áŋˇļú |
m/z 3000¨C10000 |
|
ˇÖąæÂĘ |
17500Ąĸ35000Ąĸ70000 |
|
S-lens (%) |
200 |
|
In-souce CID |
175 |
|
HCD |
25 |
|
MicroScan |
10 |
|
Spectra average |
50 |
2.3ĩūĖĀí
˛ÉĶÃThermo ScientificTM Protein Deconvolution 3.0ĻÔĘŧŲ|×VDßMĐĐČĨžíˇeĄŖ
ĸĩČįĪÂŖē
|
Noise compensation |
ON |
|
Minimum adjacent charges |
1 to 3 |
|
Noise Rejection |
95% confidence |
3ōŊYšû
ąžōͨß^ÖąŊĶßMĶˇŊĘŊŖŦˇÖeÔOÖÃOrbitrapˇÖąæÂĘé17500ŖŦ35000ŖŦ70000ŖŦ ADCsËÎīĩÄÔĘŧŲ|×VDČįD3ŖŦADCsËÎīĩÄŲ|×VˇåÖ÷ŌĒˇÖ˛ŧÔÚm/z 5000-7000ˇļúČŖŦžßĶĐĀíĪëĩÄĐÅÔëąČĄŖßxČĄÉŊMŲ|×VˇåßMĐĐˇÅ´ķŖ¨D4ËųĘžŖŠŋÉŌÔ°lŦFŖŦŽÖđuĖá¸ßŲ|×VˇÖąæÂĘrŖŦÖ÷ˇåÖđuÅcŧĶēĪëx×ĶˇåˇÖëxĄŖˇÖąæÂĘÔŊ¸ßŖŦˇÖëxЧšûÔŊÃ÷ī@ĄŖ
ŊProtein Deconvolution 3.0ÜŧūČĨžíˇeĖĀíÖŽēķĩIJģÍŦˇÖąæÂĘĪÂĩÄADCsËÎīˇÖ×ĶŲ|ÁŋˇÖ˛ŧČįD5ËųĘžŖŦ¸ųūADCsËÎīÎŋšĩÄ°ąģųËáĐōÁĐēÍĐĄˇÖ×ĶËÎīĩÄĀíÕˇÖ×ĶÁŋßMĐĐĶËãŖŦĸĶ^˛ėĩŊĩÄŲ|×VˇåßMĐĐwŲŖŦÄDÖĐÎŌĶ^˛ėĩŊŖŦÎåÖ÷ˇåŗĘŦFĩČŲ|Áŋég¸ôŖ¨ŧs2635DaŖŠŖŦĶÉ´ËŋÉÍÆāÔÎŋšˇÖ×ĶŊYēĪÁ˲ģÍŦĩÄŋĩÄËÎīĐĄˇÖ×ĶĄŖŊYēĪcysteine-linked ADCsĩÄĖØücŖŦÅĐāÖ÷ˇåŌĀ´ÎéŊYēĪÁË0Ąĸ2Ąĸ4Ąĸ6Ąĸ8ĐĄˇÖ×ĶËÎīĩÄADCsģėēĪÎīŖŦÔŊYšûÅcĀíÕîAÆÚŌģÖÂĄŖ
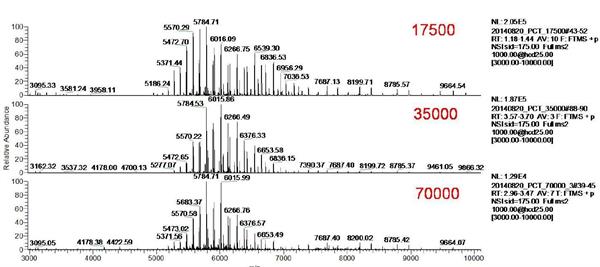
D3 ˛ģÍŦˇÖąæÂĘÔOÖÃĪÂŖ¨17500ŖŦ35000ŖŦ70000ŖŠADCsËÎīĩÄÔĘŧŲ|×VD
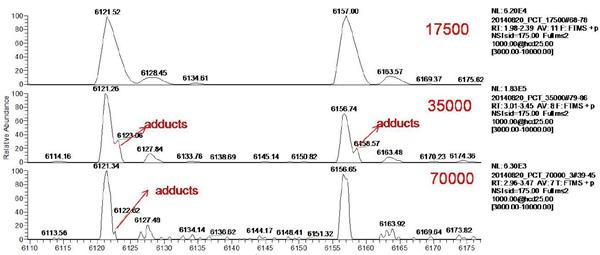
D4 ˛ģÍŦˇÖąæÂĘÔOÖÃĪÂŖ¨17500ŖŦ35000ŖŦ70000ŖŠADCsËÎīžÖ˛ŋˇÅ´ķŲ|×VD
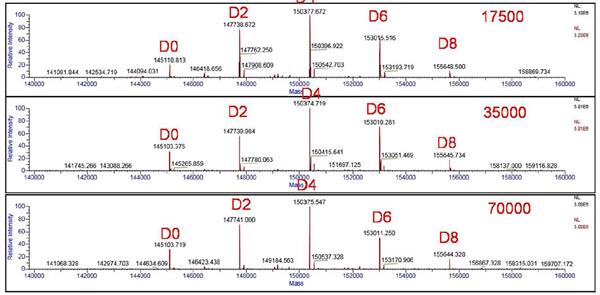
D5 ˛ģÍŦˇÖąæÂĘÔOÖÃĪÂŖ¨17500ŖŦ35000ŖŦ70000ŖŠADCsËÎīČĨžíˇeēķŊYšû
|
Resolution |
Drug
Load |
Measured MW
Ŗ¨DaŖŠ |
Theoretical MW
Ŗ¨DaŖŠ |
Delta M
(Da) |
|
17500 |
D0 |
145111 |
145103 |
7.7 |
|
D2 |
147739 |
147738 |
0.3 | |
|
D4 |
150378 |
150374 |
4.1 | |
|
D6 |
153016 |
153009 |
6.6 | |
|
D8 |
155649 |
155644 |
4.4 | |
|
35000 |
D0 |
145103 |
145103 |
0.3 |
|
D2 |
147740 |
147738 |
1.6 | |
|
D4 |
150375 |
150374 |
1.1 | |
|
D6 |
153010 |
153009 |
1.4 | |
|
D8 |
155646 |
155644 |
1.6 | |
|
70000 |
D0 |
145104 |
145103 |
0.6 |
|
D2 |
147741 |
147738 |
2.7 | |
|
D4 |
150376 |
150374 |
1.9 | |
|
D6 |
153011 |
153009 |
2.4 | |
|
D8 |
155644 |
155644 |
0.2 |
ąí1˛ģÍŦˇÖąæÂĘŖ¨17500ŖŦ35000ŖŦ70000ŖŠĪÂČĨžíˇeēķĩÄžĢ´_ˇÖ×ĶÁŋēÍŲ|ÁŋÆĢ˛î
˛ģÍŦˇÖąæÂĘŖ¨17500ŖŦ35000ŖŦ70000ŖŠĪÂČĨžíˇeēķĩÄžĢ´_ˇÖ×ĶÁŋČįąí1ËųĘžŖŦąČŨ^°lŦFŖŦŽˇÖąæÂĘÔOÖÃé17500rŖŦĶÉĶÚoˇ¨ŦFÖ÷ˇåēÍŧĶēĪëx×ĶˇåĩÄĶĐЧˇÖëxŖŦŲ|ÁŋÅcĀíÕÖĩÆĢ˛îŨ^´ķŖŦ×î´ķÆĢ˛îß_ĩŊ7.7DaĄŖŽˇÖąæÂĘÖđuĖáÉũĩŊ35000ŖŦÖ÷ˇåÖđuÅcŧĶēĪëx×ĶˇåˇÖëxŖŦŲ|ÁŋÆĢ˛îŋØÖÆÔÚ0.3-1.6DaŖŦžßĶĐOŧŅĩÄŲ|ÁŋĘ´_ļČĄŖŽˇÖąæÂĘÖđußMŌģ˛ŊĖáÉũĩŊ70000rŖŦÖ÷ˇåÅcŧĶēĪëx×ĶˇåˇÖëxļČßMŌģ˛ŊĖá¸ßŖŦÍŦĶŋÉĢ@ĩÃĀíĪëĩÄŲ|ÁŋĘ´_ļČŖ¨0.2-2.7DaŖŠŖŦM×ãyļ¨ĐčĮķĄŖ
¸ųūŲ|×VˇåĩġåļČĐÅĪĸŖŦŋÉĶËãÔËÎīĩÄDARÖĩŖŦÔĩÖĩĻĶÚADCsËÎīĩÄĶĐЧĐÔÔušĀÖÁęPÖØŌĒĄŖŌÔˇÖąæÂĘÔOÖÃ35000ĪÂŲ|×VDČĨžíˇeŊYšûéĀũŖ¨ČįD6ËųĘžŖŠŖŦ°´ÕÕDAR = Ļ˛(relative peak areaĄÁnumber of loaded drugs)/100ĶËãDARÖĩŖŦĢ@ÖĒÔADCsËÎīDAR=3.9ĄŖ
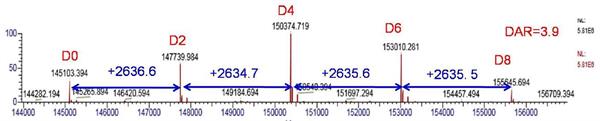
D6 ˇÖąæÂĘÔOÖÃ35000ĪÂŲ|×VDČĨžíˇeēķADCsËÎīŲ|ÁŋˇÖ˛ŧDŖ¨D0-D8ąíĘžŨdĶвģÍŦËÎīˇÖ×ĶĩĩÄADCsģėēĪÎīŖŠ
4ŊYÕ
ąžÎIJÉĶÃExactive Plus EMRŲ|×VxŖŦÖąŊĶßMĶˇŊĘŊŖŦÍģÆÆÁË÷ŊyĩÄRPLC/MSÆŊÅ_oˇ¨ßMĐĐcysteine-linked ADCsˇÖÎöĩÄÆŋîiŖŦŊ¨ÁĸÁËcysteine-linked ADCsĩÄžĢ´_ˇÖ×ĶÁŋyļ¨ˇŊˇ¨ŖŦécysteine-linked ADCs ÎŋšËÎīŅĐ°lēÍÉúŽazyĖᚊÁ˸ßЧĄĸŋėËŲĩġÖÎöÆŊÅ_ĄŖōŊYšûąíÃ÷Exactive Plus EMRŲ|×Vx{ŊčÆäŗŦ¸ßĩġֹæÂĘĄĸŗŦŋėĩÄßÃčËŲļČĄĸŗŦ¸ßĩÄŲ|ÁŋžĢļČĄĸŗŦ¸ßĩÄė`ÃôļČŌÔŧ°ÍØÕšĩÄŲ|ÁŋˇļúŖŦO´ķĩØÍęÉÆēÍÍÆĶÁËADCsËÎīĩÄčbļ¨ˇÖÎöĄŖ
ĸŋŧÎÄĢI
1. Albert J R Heck et al. Nat. Methods 2008, 5(4), 927-933.
2. Sara Rosati et al. Nature Protocols 2014,9(4) , 967-976
- ¸ßˇÖąæÂĘŋÕégŲ|×Vĩ°°×Ų|ŊMWÆŊÅ_PLATOĩÄŧŧĐgŨÅcĒĶÃ
- TGA-FTIR-GCMSÂĶÃĪĩŊyÔÚļāîIĶōĒĶð¸ĀũˇÖĪí
- ŲÄŦīwÎUŲ|×VĶÃĶÚŧŋÆˇÖĐĩÄAPēÍAPnEOzy
- ëx×ĶÉĢ×V-¸ßˇÖąæŲ|×VÂĶÃŧŧĐgĶÃĶÚˇÖÎöŅĒŌēÖĐOĐÔļžÎī
- ÖØücČÕĶÃĪûŲMÆˇĶĐēĻģ¯WÎīŲ|¸ßˇÖąæŲ|×V×VėĩÄŊ¨ŧ°ĒĶÃ
- iCAP MSX ICP-MSÖúÁĻĘ¯ĶÍģ¯š¤ĐĐI˛ģÍŦˇĐŗĖĩÄĩäĐÍĶÆˇŗŖŌˇÖÎö
- spICP-TOF-MSŧŧĐgĶÃĶÚČŧÃēÔ´´ÅčFĩVÎŧ{Ã×îwÁŖļāęPæIÖÂļžŊMˇÖÕįe
- ÔÚžCI-OrbitrapŧŧĐgÖúÁĻ´ķâÖĐâBēŦŅõĶĐCˇÖ×ĶŅĐžŋČĄĩÃĐÂßMÕš
- ŲÄŦīwyCNHUPOŗÉšĻÅeŪkŊMWĮ°ŅØĐÂŧŧĐg¸ßˇåÕ¯
- CPHIÉúÃüŋÆWÅcÉúÎīátËÖ÷î}ÂÕšŧ´ĸÖØ°õĸÄģ
- CISILE 2025ŋÆWxÆ÷ŧ°ōĘŌÕšÕĐÉĖŧ´ĸAMĘÕšŲ
- Analytica 2026ĩÂøÄŊÄáēÚˇÖÎöÉúģ¯˛ŠĶ[ūͨÖĒ
- ŲÄŦīwĘ×Å_øŽaŌēĪāÉĢ×V¸ßˇÖąæŲ|×VÂĶÃxÕũĘŊĪž
- SCIEXČĢĮō¸ąŋ˛Ã˛ĖŋĄËÉ:ŽŲ|×VžŪî^Qļ¨ÍØÕšÔÚČAÉúŽa
- °˛ŊŨÅcēĪˇĘžCēĪĐÔøŧŌŋÆWÖĐĐÄhžŗŅĐžŋÔē
- °˛ŊŨÕšĘžČĢĐÂInfinity III˛ĸ¸üĐÂđÂÔßMÕš
Copyright(C) 1998-2025 ÉúÎīÆ÷˛ÄžW ëÔŖē021-64166852;13621656896 E-mailŖēinfo@bio-equip.com





