NaicaĩŨÖPCRžžÐgĶNSCLCŧžÕßŅŠ{ÖÐEGFRÏāęPÍŧŨzyĩÄŠÓÃ
·ĮÐĄž°û·Î°ĐĢĻNSCLCĢĐ
·Î°ĐĘĮĘĀ―įÉÏŨîģĢŌĩÄšÐÔÄ[ÁöÖŪŌŧĢŽŌŅģÉéÎŌøģĮĘÐČËŋÚšÐÔÄ[ÁöËĀÍöÔŌōĩÄĩÚŌŧÎŧĄĢÆäÖÐĢŽ·ĮÐĄž°û·Î°ĐžsÕžËųÓзΰĐĩÄ80%ĢŽžs75%ĩÄŧžÕß°lŽFrŌŅĖÓÚÖÐÍíÆÚĢŽ5ÄęÉúīæÂĘšÜĩÍĄĢ
ķø·ĮÐĄž°û·Î°ĐÖÐŨîģĢŌĢŽĮŌÓÐáĶÐÔ°ÐÏōËÎïĩÄÍŧŨūÍĘĮ“ąíÆĪÉúéLŌōŨÓĘÜów”ĢĻEGFRĢĐÍŧŨĄĢąíÆĪÉúéLŌōŨÓĘÜówEGFRŧųŌōÎŧÓÚĩÚ7ĖČūÉŦówķĖąÛÉÏĢŽŲÓÚĀŌ°ąËážĪÃļĘÜówĄĢÆäÖÐEGFRĀŌ°ąËážĪÃļ ^ÓōĩÄÍŧŨÖũŌŠ°lÉúÔÚ18ĄŦ21Íâï@ŨÓĢĻŌÏÂDĢĐĄĢŌōīËÄÜōąMÔį°lŽFNSCLCŧžÕßEGFRÍŧŨĮérĢŽūÍŋÉŌÔáĶÐÔĩÄßMÐÐÏāęPÖÎŊĢŽpÝpēĄČËÍīŋāĢŽŅÓéLÉúÃüÖÜÆÚĄĢ
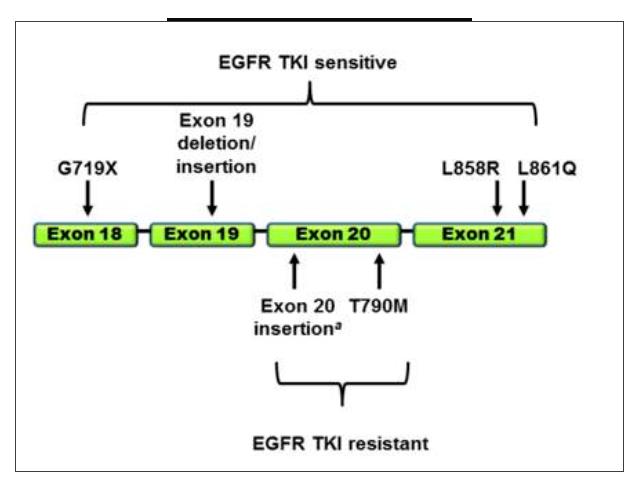
Ąø EGFRģĢŌÍŧŨÎŧüc
ĩŨÖPCRŨũéĩÚČýīúPCRžžÐgĢŽ{―čļßė`ÃôķČĄĒļßūŦĘķČĢŽĶŌÖÖÆĐÓÐÝ^ÄÍĘÜÄÜÁĶĩČÝÕýÖðuģÉéoŅŠ{zy-ŌšówŧîzĩÄŋÉŋŋ·―·ĻĄĢČŧķøĢŽīóķāĩĮérÏÂĩŨÖPCRĩÄĩÍÍĻÁŋšÍļßģÉąūĩČŌōËØÏÞÖÆÁËÆäÔÚÅRīēzy·―ÃæĩÄŠÓÃĄĢ
°ŽÆÕ°ÝÉúÎïĢĻapexbioĢĐĩÄŅаlFę ―üČÕÔÚÖŠÃûësÖūĄķBritish Journal of CancerĄ·ĢĻBJCĢĐÉÏ°ląíÁËŌŧÆŠî}éPlasma-based early screening and monitoring of EGFR mutations in NSCLC patients by a 3-color digital PCR assayĩÄÎÄÕÂĄĢß@ÆŠÎÄÕÂÍĻß^ļßė`ÃôĩÄĩŨÖPCRžžÐgĶNSCLCŧžÕßŅŠ{ÖÐĩÄEGFRËŪÆ―ßMÐÐÍŧŨzyĢŽēĒŋÉÍŽrzyEGFRŧųŌōĩÚ18-21Íâï@ŨÓĩÄ39ÍŧŨĢŽOīóĖáļßÅRīēEGFRÍŧŨzyÄÜÁĶĢŽÓČÆäĘĮŪīýyÓąūÓÐÏÞrĢŽÔ·―·ĻŋÉÄÉŲÁŋÓąūÖÐŦ@ĩÃļüķāŧųŌōÐÅÏĒĄĢÔësÖūÓ°íŌōŨÓ5.791ĄĢĢĻÔĮéÕŌÎÄÄĐĢĐ

ŅÐūŋąģū°Ģš
ĘđÓÃĩŨÖPCRŧųÓÚoŅŠ{ĩÄEGFRÍŧŨzyÓÐÍûģÉéîAyEGFR-TKIЧÂĘĩÄŋėËŲĄĒė`ÃôšÍŋÉŋŋĩÄ·―·ĻĄĢČŧķøĢŽĩŨÖPCRĩÄĩÍÍĻÁŋšÍļßģÉąūÏÞÖÆÁËÆäÔÚÅRīē·―ÃæĩÄŠÓÃĄĢ
·―·ĻĢš
ŅÐūŋÕßÔOÓÁËŌŧ·NĩŨÖPCR·―·ĻĢŽŋÉŌÔÍŽrzyEGFRŧųŌō18-21ĖÍâï@ŨÓĩÄ39ÍŧŨĄĢéÁËßMÐÐļüČŦÃæĩÄÔuđĀĢŽĘÕžŊÁË30ĀýNSCLCŧžÕßĩÄŧØîÐÔFFPE―MŋšÍ33ĀýNSCLCŧžÕßĩÄŅŠ{ßMÐзÖÎöĄĢ
―YđûĢš
ĘđÓÃNaica Crystal Digital PCRžžÐgyĩÃEGFRÍŧŨzyĩÄLODé0.308 copies/μLĢŽÅcFFPE―MŋÓąūÖÐĩÄARMS-PCRzy―YđûÏāąČĢŽ33ĀýŧžÕßŅŠ{dEGFR39zyĩÄĘī_ķČé87.88%ĢĻ29/33ĢŽ95%CI 72.67-95.18%ĢĐĄĢÔÚĶ33ĀýŧžÕßßMÐÐąOyrĢŽdEGFR39ÔuđĀĩÄEGFRÍŧŨÅcÖÎŊĩÄŋÍÓ^·īŠÏāęPĄĢ
īËÍâĢŽdEGFR39ąČSuperARMS PCRÄÜļüÔįîAyTKIÖÎŊšóÄÍËĩÄNSCLCŧžÕßĩÄÅRīēîAšóĄĢÓÃdEGFR39Ķ8ĀýŧžÕßĩÄ13ĀýÓąūßMÐÐÁËčbķĻĢŽß@ÐĐÓąūëSrégÍÆŌÆūßÓÐT790MÍŧŨĢŧĶß@13ÓąūÍŽrßMÐÐSuperARMSzyĢŽHÓÐ9ĢĻ69%ĢĐąŧzģöĄĢēÉÓÃIcotinibÖÎŊ368ĖėšóĢŽÔÚŧžÕßP-15ĩÄŅŠ{ÖÐÍŽrzyĩ―L858RšÍT790MÍŧŨĄĢČŧķøĢŽSuperARMS PCRÎīÄÜzyĩ―T790MÍŧŨĢŽīËÍâĢŽÖąĩ―121ĖėCT―YđûēÅÓÐÃũï@ĩÄßMÕđĄĢÍŽÓĢŽÔÚŧžÕßP-25ÖÐĢŽdEGFR39―Yđûï@ĘūÔÚTKIÖÎŊ251ĖėšóĢŽ19DelšÍT790MĩÄÍŧŨØSķČÔöžÓĢŽąČÓ°ÏņWßMÕđĖáĮ°43ĖėĄĢÔÚŧžÕßP-23ÖÐĢŽŌēģöŽFÁËÏāËÆŽFÏóĄĢūCÉÏËųĘö, dEGFR39 zyT790MÍŧŨĩÄ°lÉúŌŠÔįÓÚSuperARMS PCRšÍCTģÉÏņĢŽß@ŌŧücŋÉÔÚÔ\āšÍîAšóÖаl]ÖØŌŠŨũÓÃĄĢ
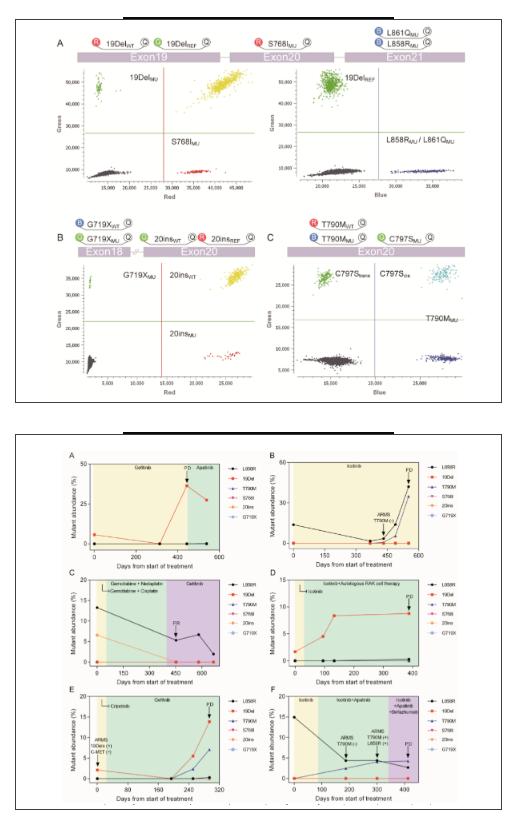
―YÕĢš
Ô―YđûąíÃũĢŽdEGFR39·ÖÎöĘĮŋÉŋŋĢŽė`ÃôĩÄĢŽēĒŋÉOīóĩÄđĘĄzyģÉąūĄĢīË·―·ĻÓÐÖúÓÚĶEGFRÍŧŨßMÐÐķāÖØ·ÖÎöĢŽŌÔßMÐÐTKIÖÎŊšóĩÄūŦÃÜąOyšÍ°éëSÔ\āĢŽÓČÆäßmÓÃÓÚ―MŋŧîzÓąūÝ^ÉŲĩÄŧžÕߥĢ
NaicaĩŨÖPCRÆ―Å_
·ĻøStilla TechnologiesđŦËūĩÄNaicaĩŨÖPCRžžÐgÔÚßMÐКËËázyrūßÓЊĖØĩÄÝĄĢÏĩ―yĀûÓÃcutting-edgeÎĒÁũówÐÂÐÍÐūÆŽ—SapphireÐūÆŽŨũéĩŨÖPCRß^ģĖĩÄÎĻŌŧšÄēÄĄĢÓÆ·ÍĻß^ÃŦžÍĻĩĀūWļņŌÔ30,000ÎĒĩÎĩÄÐÎĘ―ßMČë2DÐūÆŽÖÐĄĢ3ÉŦÉđâzyxÆũĢŽÕûÁũģĖÖŧÐčŌŠÉ°ëÐĄrĢŽēĒŋÉßMÐÐĩþĩÄŲ|ŋØšÍ―YđûŨ·ËÝ·ÖÎöĢŽŦ@ĩÃĩÄĩþÕæŋÉŋŋĄĢ

ÆÚŋŊ―é―BĢš
British Journal of CancerÓÚ1947Äęé_Ęžģö°æĢŽÔësÖū°üĀĻĶÕû°Đ°YîIÓōĩÄŅÐūŋĢŽ°üĀĻÄ·ÖŨÓšÍCĀíŅÐūŋĩ―ž°ûÉúÎïWĢŽēĄĀíWĢŽōŊ·ĻĢŽÁũÐÐēĄWšÍÅRīēŅÐūŋĩÄÃčĘöĢŽĘĮąŧŌýÓÃīÎĩŨîķāĩÄ°Đ°YŅÐūŋësÖūÖŪŌŧĢŽÔÚÅRīē°Đ°YŅÐūŋ·―ÃæÓÐÖØīóØŦIĄĢ
ÔÎÄæ―Ó: https://doi.org/10.1038/s41416-020-1024-2
- ÐÂļßëAķāÖØĩŨÖPCRŋėËŲzyPIK3CAáücÍŧŨĩÄ·―·Ļ
- ÐÂļßëAķāÖØĩŨÖPCRžžÐgŠÓÃĢšÅRīēČéÏŲ°ĐERBB2ŧųŌōÍŧŨŌšówŧîz
- ÐÂļßëAķāÖØĩŨÖPCRŽF·ĮÐĄž°û·Î°ĐEGFR 19·NÍŧŨūŦĘÅRīēzy
- ÐÂļßëAķāÖØĩŨÖPCRžžÐgÖúÁĶČéÏŲ°ĐESR1ÍŧŨÅRīēūŦĘzy
- ÁųÖØĩŨÖPCRzy·―·ĻÖúÁĶÞDŧųŌōŋėËŲĄĒĘī_ĄĒūŦĘķĻÁŋzy
- ŌšówŧîzŠÓÃĄ°Crystal Digital PCRĄąļßëAķāÖØžžÐgßMÐзš°ĐÍŧŨzy
- ĩŨÖPCRÔÚķĻÁŋMSC-exÖÐmiR-27b-3ÖúÁĶļÎĀwūSŧŊŅÐūŋĩÄŠÓÃ
- ČŦŨÔÓĩŨÖPCRļßëAķāÖØzyÔÚČéÏŲ°ĐESR1ÎŋŨ12ÖØŧųŌōÍŧŨķĻÁŋĩÄŠÓÃ
- °ŽÆÕ°ÝqMate miniÐÂÆ·ÉÏĘÐĢŽČŦÃæēžūÖ·ÖŨÓzyŪaÆ·ū
- °ŽÆÕ°ÝūW―jŅÐÓþîAļæĢšĩŨÖPCRÔÚÅRīēÔ\āÖÐĩÄŠÓÃ
- ÍŧÆÆOÏÞĢšÐĄšĢýÍÆģöģŽķāÖØĩŨÖPCRķĻÖÆŧŊé_°l·þÕ
- ūW―jŅÐÓþĢšĩŨÖPCR·―·ĻÔuđĀÉúÎïWÄęýg
- ÐĄšĢýĩŨÖPCRÐÂÆ―Å_SCI Digital ProÕýĘ―°lēž
- °ŽÆÕ°ÝÉúÎïūŦēĘÁÁÏāĩÚËÄÃCIBMÉúÎïÓÁŋ°lÕđīóþ
- °ŽÆÕ°Ý ĒžÓĩÚķþÃÞrIÉúÎïžžÐgŪaÆ·zyžžÄÜŧîÓ
- ļĢĀûŧîÓĢšßīaÏÂÝdŌŧĖėÍęģÉļïÐÂ16SyÐōĘÖÔ





