無動物源性:新型植物源成分在CGT研發與生產中的應用

近幾年細胞基因治療 (Cell and Gene Therapy, CGT)在癌癥、代謝類疾病、退行性疾病以及先天遺傳性疾病等治療方面取得了突破性成果,也是現在最火熱的治療技術之一,國家也陸續出臺多項政策促進CGT的進步發展。2020年5月,國家發改委印發《“十四五”生物經濟發展規劃》,在第(五)部分“加快提升生物技術創新能力”的“開展前沿生物技術創新”中提到:發展基因診療、干細胞治療、免疫細胞治療等新技術,強化產學研用協同聯動,加快相關技術產品轉化和臨床應用,推動形成再生醫學和精準醫學治療新模式。
一、細胞基因治療技術分類
細胞治療:指利用患者自身或供者來源的細胞,經過體外分離純化、培養擴增、活化或基因修飾、基因編輯等操作,再回輸到患者體內,從而達到治療疾病的治療方式。從細胞類型上區分,細胞治療主要可分為免疫細胞治療、干細胞治療和其它體細胞治療。
基因治療:基因治療是一種利用基因載體將外源的正常基因或有治療作用的基因導入靶細胞,或用具有正常功能的基因置換/增補患者體內有缺陷的基因,從而達到治療疾病的方法。從載體形式上區分,基因治療相關技術可分為病毒載體編輯技術和非病毒載體的編輯技術。
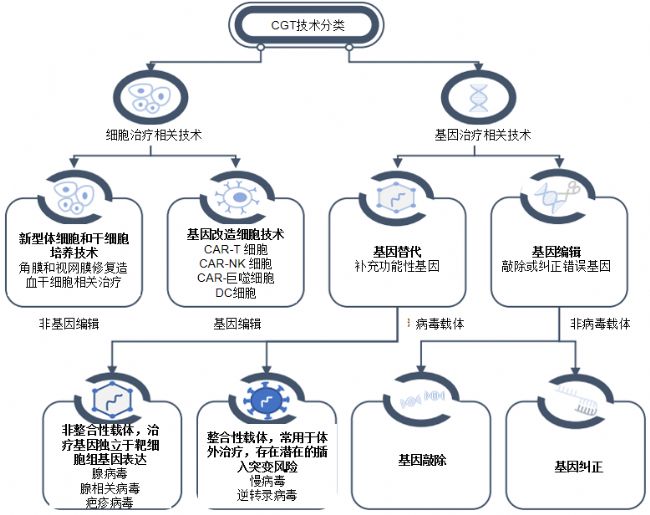
圖1:CGT技術分類(來源:沙利文分析)
二、動物來源原輔料在CGT中的安全性問題
2010年葛蘭素史克公司(GSK)生產的輪狀病毒(Rotavirus,RV)疫苗 Rotarix 中被檢測出I型豬圓環病毒(Porcine circovirus,PCV)的DNA片段[1],不久FDA發布消息稱在 Rotarix 中檢出了外源性病毒成分,因此,建議暫時停止使用該疫苗。該事件引發了人們對動物源性原材料可能會給生物制藥帶來嚴重的安全隱患的思考。
CGT生產過程如細胞培養、細胞庫開發等階段中會用到一些動物源的原輔料,比如血清(人源)、人血白蛋白(人源)、胎牛血清(牛源)以及胰酶(豬源)等,因此可能存在將一些動物源性的病毒因子引入到終產品的風險,而這些動物源性病毒因子最終可能會隨著CGT藥品一同被輸送至患者體內,從而引發相關的傳染性疾病。這些動物源性的病毒因子除了給患者造成身體損害,也給CGT生產企業造成巨大壓力和經濟損失,因為CGT產品生產的各個階段都需要做嚴格的病毒檢測,這些檢測既是CGT行業質量控制的重要指標,同時也給生產企業增加了生產成本。
2020版中國藥典中強調:“對于不同風險級別原材料的質量控制,應充分考慮來源于動物(或人)的生物原材料可能帶來的外源因子污染的安全性風險。而對于高風險等級的原材料,應在產品研發的早期評價使用這些原材料的必要性,并尋找其他替代物或替代來源。”[2]
另有多個CGT相關行業技術指導原則特別指出在CGT生產過程中應盡可能避免使用動物源性原輔料:
表1. CGT相關行業技術指導原則中對動物源原輔料的要求
| 發布時間 | 發布機構 | 技術指導名稱 | 具體要求內容 |
| 2015 | CDE | 《干細胞制劑質量控制及臨床前研究指導原則》(試行)[3] | 除特殊情況外,應盡可能避免在干細胞培養過程中使用人源或動物源性血清,不得使用同種異體人血清或血漿。如必須使用動物血清,應確保其無特定動物源性病毒污染。嚴禁使用海綿體狀腦病流行區來源的牛血清。應結合體內和體外方法,根據每一細胞制劑的特性進行人源及動物源性特定致病因子的檢測。如使用過牛血清,須進行牛源特定病毒的檢測;如使用胰酶等豬源材料,應至少檢測豬源細小病毒;如胚胎干細胞和iPS細胞在制備過程中使用動物源性滋養細胞,需進行細胞來源相關特定動物源性病毒的全面檢測。另外還應檢測逆轉錄病毒。 |
| 2017 | CDE | 《細胞治療產品研究與評價技術指導原則》(試行)[4] | 細胞培養過程中,應盡量避免使用動物或人來源的物質,比如應盡量避免血清的使用,若必須使用血清,需要提供相關的研究資料說明使用的必要性和合理性;嚴禁使用疫病流行區來源的動物血清;不得使用未經過安全性驗證的血清。 |
| 2023 | CDE | 《腺相關病毒載體類體內基因治療產品臨床試驗申請藥學研究與評價技術指導原則》(試行)[5] | 原材料和輔料的質量控制可參照《中國藥典》通則“生物制品生產用原材料及輔料質量控制”的相關要求,質控策略應與其風險相符。如有可能,應盡量避免使用動物源或人源性原材料。如需使用,需提供相關的必要性和合理性證明,并制定相應的風險控制措施。 |
CGT制品生產過程復雜而精細,任何關鍵步驟的細微變化均可能引起終產品性能的改變,而動物源原輔料除了存在外源性病毒風險之外,還存在來源多樣、成分復雜、批間差控制難度大等問題,這些對CGT制品的質量、穩定性以及安全性都會造成影響。因此,動物源性也是CGT監管申報存在的主要問題之一。這也導致無血清、無動物源性的原輔料也越來越被行業普遍接受。
三、植物源原輔料在CGT研發與生產中的優勢
禾元生物依托自己的專利技術平臺—— 水稻胚乳細胞生物反應器高效重組蛋白質表達平臺(OryzHiExp)和重組蛋白純化技術平臺(OryzPur)開發了一系列適合CGT研發與生產的原輔料:
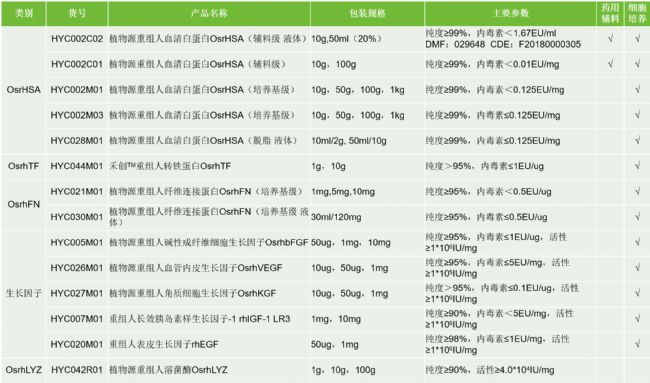
上述產品均不含有任何人或動物來源的成分,在CGT研發或生產中具有以下優勢:
- 安全性好,消除動物來源或血液制品中病毒和其他未知因素的潛在風險;
- 高批間一致性,提高了細胞培養和實驗結果的重復性;
- 質量可控,排除動物來源的末知成分與含量不明確蛋白造成的批間差;
- 供應穩定,產能充足;
- 成分明確,簡化下游生物加工或生物研究;
- 高純度,低內毒素,低雜質
禾元生物植物源原輔料相較于動物源原輔料可以增加CGT產品批與批的質量穩定性,提高產品的安全性,以及更簡化的監管途徑( Regulatory Friendly)!
參考文獻:
[1] Victoria JG,Wang CL,Jones MS,et al. Viral nucleic acids in live-attenuated vaccines: detection of minority variants and anadventitious virus[J]. J Virol,2010
[2]《生物制品生產用原材料及輔料質量控制》,2020版中國藥典
[3]《干細胞制劑質量控制及臨床前研究指導原則》(試行)
[4]《細胞治療產品研究與評價技術指導原則》(試行)
[5]《腺相關病毒載體類體內基因治療產品臨床試驗申請藥學研究與評價技術指導原則》(試行)
參考文獻:
[1] Victoria JG,Wang CL,Jones MS,et al. Viral nucleic acids in live-attenuated vaccines: detection of minority variants and anadventitious virus[J]. J Virol,2010
[2]《生物制品生產用原材料及輔料質量控制》,2020版中國藥典
[3]《干細胞制劑質量控制及臨床前研究指導原則》(試行)
[4]《細胞治療產品研究與評價技術指導原則》(試行)
[5]《腺相關病毒載體類體內基因治療產品臨床試驗申請藥學研究與評價技術指導原則》(試行)
Copyright(C) 1998-2025 生物器材網 電話:021-64166852;13621656896 E-mail:info@bio-equip.com





