植物來源的類外泌體納米囊泡的研究進展與展望
外泌體是一種小的細胞外囊泡,大小從30~150納米不等,可以來源于各種類型的細胞。近年來,哺乳動物來源的外泌體被廣泛研究,并發現在調節細胞間通信中發揮關鍵作用,從而影響多種疾病的發展和進展。數千年來,傳統中醫一直在使用植物性藥物,越來越多的證據表明,植物來源的外泌體樣納米囊泡(植物外泌體)在結構和功能上與哺乳動物來源的外泌體有相似之處。在這篇綜述中,概述了植物外泌體研究的最新進展及其對人類健康的潛在影響。具體來說,總結了在呼吸、消化、循環和其他疾病中的作用。植物外泌體作為一個有前途的研究領域的潛力,對人類疾病的治療具有廣泛的意義。我們將持續探索植物外泌體對人類健康的影響。

然而,外泌體存在局限性,包括同時含有免疫激活劑和免疫抑制因子,可能會降低宿主對病原體的抵抗力,以及提取難度高、純度低,這大大增加了外泌體生產成本。通過改進提取工藝和擴展可用性來克服這些限制來源是必要的,這導致了植物來源的外泌體樣納米囊泡(PELNs)的發現。根據目前的研究,植物細胞外囊泡的生物發生有三種可能的途徑:外囊陽性細胞器(EXPO)途徑、多泡體(MVBs)途徑和液泡途徑。其中,MVBs途徑被認為是PELNs形成的主要途徑。基本過程包括質膜向內出芽以形成早期內體,這些內體成熟并與反式高爾基體網絡通信,形成MVBs。MVBs內的腔內囊泡(ILV)可以包含各種物質,如RNA、DNA、脂質等。MVBs與質膜融合后,ILV可釋放到細胞外間隙,形成PELNs。該途徑與已知的哺乳動物來源外泌體(MDEs)的生物發生途徑高度相似。EXPO途徑涉及形成類似于自噬體的雙膜結構,它可以與質膜融合,向細胞壁釋放單膜囊泡。液泡途徑主要發生在植物防御真菌病原體期間。感染后,液泡與質膜融合并釋放其水解酶和防御蛋白的內容以抵消病原體的入侵。已經發現,從植物中提取的PELNs,如生姜、人參、小麥、紅景天、甘草等,不僅具有與MDEs相似的抗纖維化、抗病毒、抗腫瘤作用,而且還彌補了它們的不足,如部分免疫原性和有限來源。因此,PELNs具有很大的研究價值。
本文整理和總結了當前關于PELNs的研究,分析了PELNs的分離、純化、鑒定和功能。主要強調的是它們對臨床疾病的治療潛力,根據人體解剖系統進行分類。目標是為PELNs在臨床疾病治療中的未來利用提供綜合資源,同時也提出新的概念和研究方法,以促進對PELNs的進一步研究。
1.1 PELNs的提取
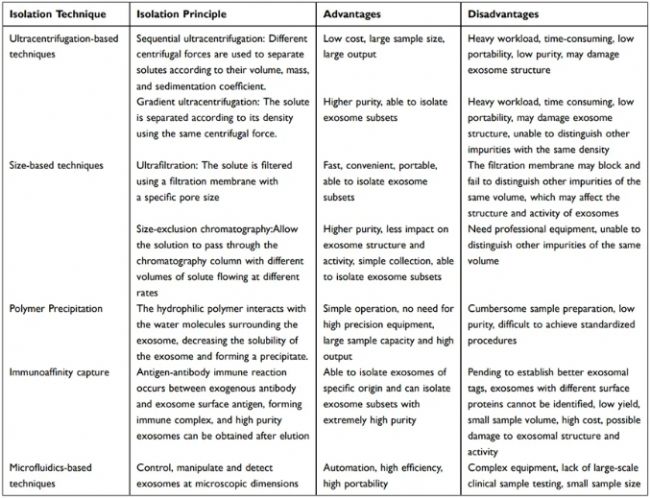 圖2 不同植物外泌體提取方法的原理、優缺點
圖2 不同植物外泌體提取方法的原理、優缺點
PELNs具有產量高、易于獲取等優點。然而,目前對PELNs提取和純化的研究大大落后于MDEs。分離和純化PELNs的可用方法相對有限,主要基于用于MDEs的成熟技術。雖然MDEs通常從生物體液中分離出來,但PELNs是從質外體清洗液中分離出來的,差速離心仍然是兩者的基本提取方法。然而,由于植物和動物之間的生理差異,通過這種方法獲得的PELNs通常與蛋白質、核酸聚集體和其他囊泡混合。因此,必須使用密度梯度超速離心法進行進一步純化以分離污染物。植物汁液中存在高分子量成分,如纖維素和淀粉,通常會導致離心困難。為了提高分離效率并解決傳統離心技術的某些局限性,研究人員提出了各種離心方法的組合。一種廣泛使用的方法將差速離心與蔗糖密度梯度離心相結合。這種方法因其易用性、經濟性和實現高提取純度的能力而廣受歡迎。按照這種方法,細胞外囊泡通常位于30%~45%蔗糖溶液的中間層,如圖3所示。
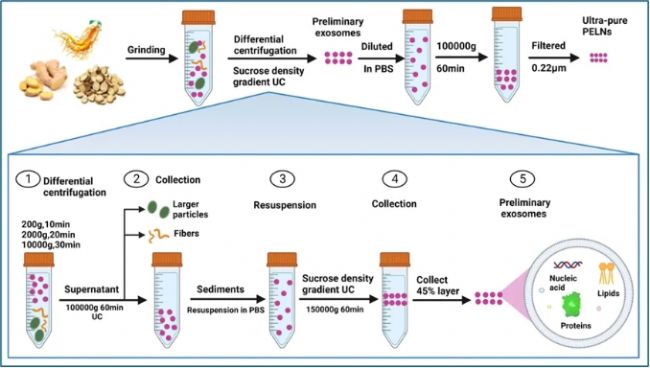 圖3 植物來源的類外泌體納米囊泡(PELNs)提取方法:超速離心結合蔗糖密度梯度離心
圖3 植物來源的類外泌體納米囊泡(PELNs)提取方法:超速離心結合蔗糖密度梯度離心
測量PELNs尺寸和表面電荷的最常用方法是動態光散射(DLS)和納米顆粒跟蹤分析(NTA)。DLS由于其分辨率低和無法測量顆粒濃度等局限性,已逐漸被NTA取代。NTA捕獲10~2000nm尺寸范圍內細胞外囊泡的布朗運動,并使用愛因斯坦方程計算它們的濃度和流體動力學直徑。它提供比DLS更高的分辨率,并且不易受到較大顆粒強烈散射的干擾,從而獲得更穩定的結果。因此,它已成為表征PELNs尺寸的首選技術。目前已知的PELNs尺寸范圍在50~500nm之間,表面電荷范圍為中性至−50mV。然而,當應用于PELNs檢測時,PELNs的不當提取會引入來自細胞碎片、脂質囊泡、膠體顆粒、蛋白質聚集體和樣品中其他雜質的污染,不可避免地影響NTA分析的結果。此外,近年來,學者們發現局部表面等離子體共振(LSPR)技術在用于外泌體檢測時表現出高靈敏度。此外,基于AFM和LSPR的細胞外囊泡表征技術在液體活檢中的應用正在得到廣泛研究。
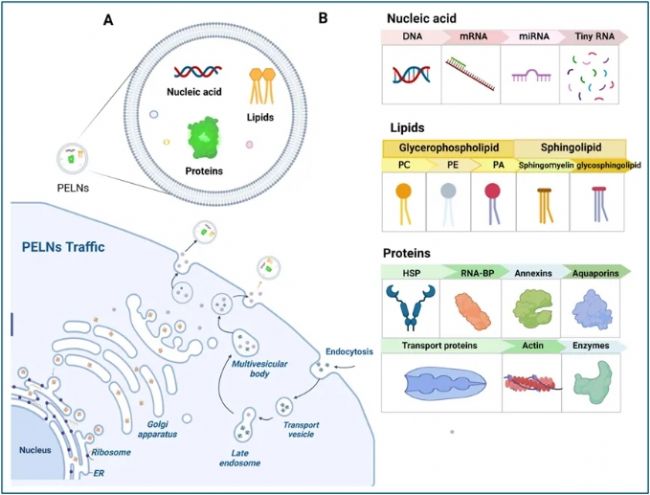 圖4 植物來源的類外泌體納米囊泡(PELNs)的生物發生、形態結構和組成
圖4 植物來源的類外泌體納米囊泡(PELNs)的生物發生、形態結構和組成
PELNs的形態和結構特征如圖4所示。與MDEs類似,PELNs的膜由磷脂雙層組成。然而,PELNs表現出不同的脂質特性,例如高濃度的磷脂酸、磷脂酰膽堿、二乳糖基二酰基甘油和單半乳糖基二酰基甘油,這與MDEs不同。這些獨特的脂質組成賦予PELNs固有的細胞調節特性。PELNs中的蛋白質濃度通常很低,并且這些蛋白質中的大多數是胞質蛋白,包括肌動蛋白、蛋白酶和膜蛋白,它們在膜內充當通道和轉運蛋白。此外,外泌體上表面標志蛋白的存在在其鑒定、表征和特異性抗原抗體反應中起著至關重要的作用。例如,CD81、CD9、CD63、TSG101和flotillin是廣泛認可的MDEs表面標志蛋白。然而,PELNs表面標志蛋白的鑒定仍然難以捉摸。盡管研究在包括葡萄柚在內的各種植物中發現了幾種高豐度的蛋白質,如髕蛋白-3、熱休克蛋白(HSP)、水通道蛋白(AQP)、網格蛋白重鏈(Chc)和甘油醛-3-磷酸脫氫酶(GAPDH),但它們的同源物已在MDEs中報道。值得注意的是,最近的研究表明,合成蛋白PEN1、ABC轉運蛋白PEN3和跨膜四蛋白-8可能是PELNs的候選表面標志蛋白。已在擬南芥中鑒定出PEN1,其在PELNs中的富集已通過Westernblot分析得到證實。已在擬南芥中檢測到PEN3,但尚未通過Westernblot確認。TET3是CD63的同源物,在PELNs中高度富集。然而,由于實驗數據有限,這種觀點尚未被廣泛接受,有待進一步研究驗證。PELNs中的核酸包括DNA和各種RNA,其中microRNA(miRNA)是一種長度為22個核苷酸的小RNA分子,缺乏編碼特性。miRNA通常調節信使RNA(mRNA)翻譯或切割mRNA以調節基因表達,或誘導特異性靶基因表達。
正是由于存在多種蛋白質、脂質、DNA和各種復合RNA,因此PELNs具有重要的特性,可以參與細胞之間的信息傳遞和材料交換,并且有許多研究將這些特性應用于人類疾病的治療(圖5),我們將在下面詳細討論。
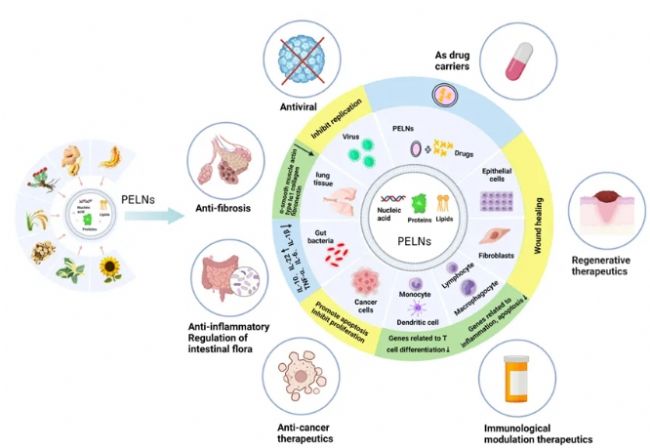 圖5 植物來源的類外泌體納米囊泡(PELNs)的生物學功能
圖5 植物來源的類外泌體納米囊泡(PELNs)的生物學功能
2.1 PELNs在消化系統疾病中的作用
例如,已發現生姜衍生的ELNs(GELNs)可以改變微生物組的組成并對宿主生理學產生積極影響。事實上,口服GELNs可以減少急性結腸炎,增加腸道修復和預防慢性結腸炎。最近的另一項研究表明,來自茶葉的ELNs可有效預防和治療小鼠的炎癥性腸病(IBD)。治療效果歸因于促炎細胞因子的下調、氧化應激的減少和腸道微生物群穩態的維持。同樣,葡萄衍生的ELNs被證明可以通過Wnt/β-catenin信號通路預防DSS誘導的小鼠結腸炎。來源于西蘭花的納米顆粒也被發現可以激活樹突狀細胞AMP活化蛋白激酶并保護小鼠免受結腸炎。此外,Zhuang等人的一項研究發現,GELNs通過調節TLR4/TRIF通路激活核因子紅細胞2相關因子2(Nrf2),防止酒精誘導的肝損傷。
PELNs對消化系統腫瘤也有治療作用。例如,生姜衍生的ELNs通過降低炎性細胞因子和細胞周期蛋白D1 mRNA水平以及抑制小鼠腸上皮細胞增殖,在治療結腸炎相關癌癥(CAC)方面顯示出有希望的結果。源自茶葉的ELNs也具有類似的功能。蘆筍柯欽衍生的ELNs也被發現在體外和體內抑制肝細胞癌細胞增殖。此外,柑橘檸檬衍生的ELNs還通過增加促凋亡基因的表達和降低抗凋亡基因的表達,通過激活腫瘤壞死因子相關凋亡配體(TRAIL)介導的細胞凋亡來刺激癌細胞死亡,并減少促血管生成因子,如VEGF-A、IL-6和IL-8來抑制腫瘤生長。蛋白質組學分析進一步表明,柑橘檸檬衍生的ELNs主要通過誘導乙酰輔酶A羧化酶α(ACACA)下調來發揮其抗腫瘤作用。
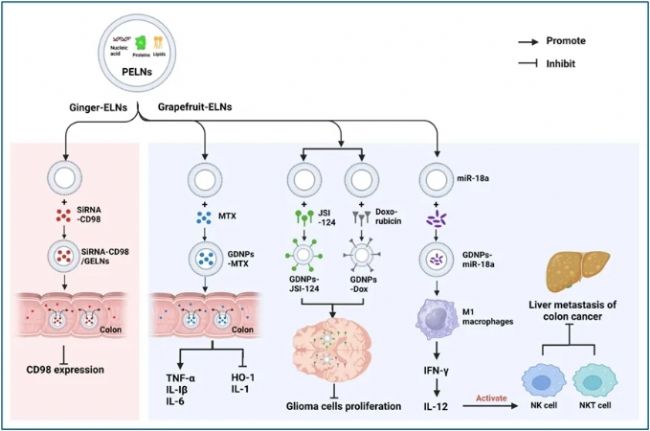 圖6 植物來源的類外泌體納米囊泡(PELNs)用作藥物遞送的載體
圖6 植物來源的類外泌體納米囊泡(PELNs)用作藥物遞送的載體
細胞外囊泡由于其高穩定性和安全性以及穿越生物屏障的能力,最近成為一種很有前途的藥物遞送載體。PELNs特別有利,因為它們是具有固有安全性、無毒和低免疫原性的天然產物(圖6)。對于炎癥性腸病,載有siRNA的生姜衍生納米脂質可有效遞送siRNA藥物以治療潰瘍性結腸炎患者。封裝在生姜衍生的口服納米脂質載體中的siRNA-CD98可以有效地靶向結腸組織并抑制CD98表達,從而減少常規合成納米顆粒對結腸疾病的副作用,同時提高特異性。同樣,已發現葡萄柚衍生的ELNs可將抗炎藥物甲氨蝶呤(MTX)遞送到炎癥部位。這種方法抑制促炎因子TNF-α、IL-1β和IL-6的產生,同時增加血紅素加氧酶-1和IL-10等抗炎因子的表達,從而提高對DSS誘導的小鼠結腸炎的治療效果。對于消化系統腫瘤,葡萄柚衍生的脂質轉化為納米載體(GNVs)已用于治療肺、結腸和乳腺腫瘤。GNVs與葉酸(GNV-FA)相結合顯著增強了它們對腫瘤的靶向性,而將抗腫瘤藥物紫杉醇(PTX)封裝在GNV-FA上允許對結腸癌進行更特異性的治療。還發現攜帶miR-18a的GNVs通過誘導IL-12表達和激活NK細胞和NKT細胞來抑制結腸癌的肝轉移。
除了對胃腸道的保護和治療作用外,還發現PELNs與牙齦卟啉單胞菌上的蛋白質特異性結合,從而降低細菌侵入人體的能力。這應用在治療慢性牙周炎方面具有潛在價值。此外,從檸檬中提取的ELNs已被證明可以提高鼠李糖乳桿菌GG和嗜熱鏈球菌ST-21的耐受性,有效抑制艱難梭菌的感染。大蒜衍生的ELNs能夠與HepG2細胞上的配體結合并被內化,從而抑制炎癥反應。香菇衍生的ELNs已被發現抑制NLRP3活化抑制IL-6的產生,同時通過降低IL1b基因的蛋白質和mRNA含量來抑制其活性,從而防止GalN/LPS誘導的急性肝損傷。
綜上所述,上述研究證明了PELNs不僅在治療消化系統疾病方面的潛力,而且在治療腫瘤方面也具有潛力。盡管大多數研究仍處于實驗室階段,需要進一步的臨床試驗,但這些發現在未來發展和臨床轉化價值方面具有巨大的潛力。
此外,植物外泌體還有望用于治療肺纖維化,肺纖維化是一種以細胞增殖、細胞外基質聚集和炎癥損傷為特征的疾病,可導致肺功能的進行性下降。近年來的研究表明,來源紅景天和蒙古蒿湯劑的植物外泌體,在體內外疾病模型中均表現出抗纖維化和抗炎作用,顯著改善小鼠肺纖維化和肺部炎癥。然而,這些作用的潛在機制尚不清楚,需要進一步的研究來闡明植物外泌體在這些疾病中的作用。
總之,PELNs在治療呼吸系統疾病(包括 COVID19 和肺纖維化)方面表現出巨大的潛力。這些發現強調了進一步探索PELNs治療應用的重要性,尤其是在呼吸系統疾病帶來的持續全球健康挑戰的背景下。
植物外泌體已被證明可以通過受體介導的細胞運輸和膜融合跨越各種生理屏障,包括血腦屏障。在一項研究中,從葡萄柚中提取的ELNs與抗腫瘤藥物阿霉素一起裝載到基于肝素的納米顆粒上,用于治療膠質瘤。結果表明,這些葡萄柚來源的ELNs可以有效地繞過血腦屏障,準確地將阿霉素轉運到腫瘤部位,從而改善抗膠質瘤的效果。葡萄柚ELNs也被發現攜帶miR17,并通過鼻內途徑抑制腦腫瘤的進展。
此外,有報道稱從人參根中提取的外泌體可以通過PI3K信號通路刺激骨髓間充質干細胞的神經分化。這一發現表明,植物外泌體可能在神經系統的再生醫學中具有巨大的潛力。
總體而言,PELN 代表了治療神經膠質瘤等神經系統疾病的一條有前途的新途徑。為了充分了解潛在機制并評估這些結果的臨床潛力,需要進行更多的研究。
研究表明,植物外泌體具有心臟保護作用。Liu等在一項研究中發現,人參根來源的外泌體可以通過保護線粒體凋亡途徑來減輕阿霉素誘導的H9C2心肌細胞損傷。植物外泌體的抗氧化作用也可以用來保護血管系統。例如,藍莓衍生的ELNs(B-ELNs)被發現通過調節TNF-α誘導的基因表達,減少活性氧(ROS)的產生和細胞活力的喪失,來防止各種應激源對血管系統的損傷。此外,B-ELNs可以作為生物活性化合物的創新候選治療載體。從油菜中分離純化的ELNs。草莓汁和檸檬在體外被脂肪間充質干細胞(ADMSCs)吸收后,具有顯著的抗氧化作用,從而促進了心臟保護作用。草莓衍生的ELNs含有大量的維生素C,據推測對氧化應激有保護作用。同時,從檸檬中提取的ELNs也被攜帶足夠數量的檸檬酸鹽和維生素C,在體外被MSC攝取后也顯示出顯著的抗氧化作用。
雖然這些研究為 PELNs 治療循環系統疾病的潛力提供了有價值的見解,但仍然缺乏臨床研究。在這些發現可以有效地應用于臨床之前,還需要進一步的研究。
Kumar等人最近的研究表明,GELNs影響芳基烴受體(AhR)的表達,AhR是一種配體激活的轉錄因子,調節體內的各種轉錄過程,包括葡萄糖代謝。AhR的過表達已經被證明會導致胰島素抵抗,而沒有AhR的小鼠則表現出更好的胰島素敏感性和葡萄糖耐量。研究小組發現GELNs誘導miR-375的表達,從而抑制AhR的表達。這導致了在小鼠之間的葡萄糖耐量和胰島素抵抗的顯著改善。同樣,從水稻糊粉蛋白細胞中提取的hvuMIR168-3p有助于人類細胞中葡萄糖轉運體1(SLC2A1)的表達上調,導致血糖水平降低。其作用的機制可能與hvu-MIR168-3p沉默線粒體電子傳遞鏈復合物I基因有關。此外,hvu-MIR168-3p可下調動物體內的低密度脂蛋白受體配體蛋白1(LDLRAP1),提高動物血液中的LDL水平。隨后的研究也表明,MIR168a的常見變異對LDLRAP1表現出不同的沉默作用。對從橙汁(ONVs)中提取的納米囊泡的治療潛力的研究已經報道了積極的結果。ONVs逆轉肥胖小鼠腸道變化,增加腸絨毛的大小,同時降低甘油三酯含量。ONVs調節幾種mRNAs的表達水平,其中一些參與免疫反應、脂肪吸收和乳糜瀉釋放。因此,ONVs可能有效預防或抑制由高脂、高糖飲食引起的與肥胖相關的胃腸道炎癥。其他研究已經探索了用納米顆粒包裹的植物提取物用于治療目的。例如,來自紫檀芪的納米顆粒制劑已被發現可以通過注射在糖尿病大鼠模型中降低血糖水平。同樣,用改良的乳液-擴散-蒸發法制備的姜黃素納米顆粒成功地降低了糖尿病大鼠模型中的空腹血糖和糖化血紅蛋白水平。最后,姜黃素納米顆粒和陳年大蒜提取物懸液在治療糖尿病心肌病、減少炎癥、心肌纖維化和心血管事件風險方面顯示出了希望。我們預計未來植物外泌體在內分泌系統疾病治療中有更多的應用。
在另一項研究中,研究人員從辣木種子中分離出MELNs,并檢測了它們治療人類急性淋巴母細胞白血病細胞和宮頸腺癌細胞的潛力。結果表明,MELNs可以抑制B細胞淋巴瘤-2(BCL-2)的表達,降低細胞內線粒體膜電位,從而抑制兩種腫瘤細胞的增殖。本研究為子宮頸癌和白血病的治療提供了一種很有前途的新方法。
總體而言,這些研究強調了 PELNs 及其 miRNA 含量作為癌癥治療策略的潛力。需要進行后續研究以優化這些分子的遞送方式,以實現最佳治療效果。
總體而言,PELNs為探索針對各種醫療條件的新治療方法提供了一條令人興奮的途徑。它們的風險較小,不會造成與干細胞移植相關的倫理問題,并且可以直接輸送到患處或靜脈注射以達到全身效果。通過持續的研究,我們可能會在未來發現這些有前途的生物活性物質的更廣泛應用。
PELNs的特性:不同的PELNs表現出不同的特性,例如大小、電荷和穩定性的變化。這些特性不可避免地對藥物加載到PELNs中的負載產生重大影響。通常,較小的囊泡具有較大的藥物載樣量,因為它們的表面積與體積比較高。它們還表現出更快的釋放速率和更高的穩定性。然而,過大和過小的囊泡都會影響載藥效率。因此,有必要開發生產大小均勻的細胞外囊泡的方法。幸運的是,研究人員已經成功地采用了Bligh和Dyer技術(一種液-液萃取方法)從PELNs中提取均勻大小的納米脂質,這些脂質作為更高效藥物遞送的載體。由于磷酸鹽的存在,PELNs通常帶有負電荷。在靜電吸引的影響下,帶正電荷的分子被這些帶負電荷或中性電荷的PELNs更有效地吸收和封裝。這為使用PELNs的載藥開辟了新的研究方向,其中可以通過改變囊泡和目標分子攜帶的電荷來提高PELNs的載藥效率。
載藥方法:目前,常用的載藥方法可分為被動負荷和主動負荷。被動加載涉及在特定溫度下將PELNs與藥物分子共孵育,依靠藥物分子和囊泡之間的擴散和親脂性相互作用進行結合。這種方法相對簡單,但包封效率可能較低。主動加載方法包括超聲輔助加載、電穿孔、擠出、和凍融循環。據報道,主動加載方法可以增加PELNs的加載能力增長了11倍以上。
外泌體修飾技術:可以通過將特定的生物活性分子固定在外泌體表面來增強外泌體遞送藥物的能力。例如,表面工程技術可用于用箭頭pRNA-3WJ和FA修飾生姜衍生的外泌體,從而增強它們將基因遞送到腫瘤部位的能力。同樣,將聚乙烯亞胺與葡萄柚衍生的外泌體雜交也可以增加它們對腦腫瘤的基因遞送能力。
給藥途徑:外泌體的給藥途徑包括口服、靜脈注射、鼻內給藥、局部注射等目前,PELNs給藥最常用的途徑是口服給藥,具有方便、易于被患者接受等優點,特別適用于胃腸道疾病的治療。但是,這種途徑存在吸收慢、接受后載藥量減少等缺點肝臟中的首過代謝。氣管輸送和靜脈注射等腸外給藥途徑可以避免上述問題,但存在呼吸道刺激或痙攣的風險以及嚴重的藥物不良反應。因此,每種給藥途徑都有其獨特的優勢和適用性,應根據不同的疾病和藥物選擇合適的給藥途徑。除了這些因素外,PELNs的載藥效率還受外泌體類型、藥物特性以及PELNs與藥物之間的相互作用等因素的影響。然而,目前該領域的研究有限,需要進一步研究。
盡管PELNs具有許多有利的生物學和物理特性,引起了研究人員越來越多的關注,但目前的研究仍然存在一定的局限性和爭議性問題。有鑒于此,我們總結了這些挑戰和爭議,并對未來的研究方向提出了建議,旨在為進一步研究PELNs提供指導。
與合成納米顆粒相比,天然PELNs在生物相容性、穩定性、體內分布、延長半衰期和細胞內化方面具有更顯著的優勢。由于它們可以根據需要加載不同類型的物質,包括小分子、核酸和重組蛋白,因此有望成為一種極具成本效益的藥物遞送平臺。
PELNs可以從豐富的植物資源中大規模生產。
參考文獻:
【1】Mu N, Li J, Zeng L. Plant-derived exosome-like nanovesicles: current progress and prospects. Int J Nanomedicine. 2023;18:4987–5009.關于納米顆粒跟蹤分析儀LighTracker






