Č~ËáĘÜķwĻÁĩÄšĻÄÜŧ°ÔÚ°Š°YÖί˛ßÂÔÖĐĩÄļāÃæĐÔĒĶÃ
Č~ËáÔÚDNAēĪŗÉēÍĐŪÍÖĐÆđÖøęPæI×÷ĶÃŖŦĻĶÚŧ°ûĩÄÔöÖŗē͡ÖÁŅÖÁęPÖØŌĒŖŦÔÚ°Š°Yŧ°ûÖĐŖŦČ~ËáÎĖŧ´úÖxĩÄŽŗŖģîģ¯ŋÉÄÜ´ŲßMÄ[ÁöĩÄÉúéLēÍ´æģîĄŖŌō´ËŖŦČ~ËáÎĖŧ´úÖxĩÄÍžŊŗÉé°Š°YÖίĩÄÔÚ°ĐücĄŖ
Č~ËázČĄCÖÆŽÖĐŖŦ×îÖØŌĒĩÄŪDß\ķw°üĀ¨ßÔĐÔČ~ËáŪDß\ĩ°°×(RFC)ĄĸŲ|×ĶņîēĪČ~ËáŪDß\ĩ°°×Ŗ¨PCFTŖŠēÍČ~ËáĘÜķw(FRα) ĄŖß@ČũˇNĩ°°×Ų|ÔÚČ~ËázČĄÖĐļŧÆđÖøęPæI×÷ĶÃŖŦĩĢĮ°ÉˇNÄŋĮ°ß˛ģĘĮŋš°ŠËÎīĩÄÖąŊĶ°ĐËĄŖ
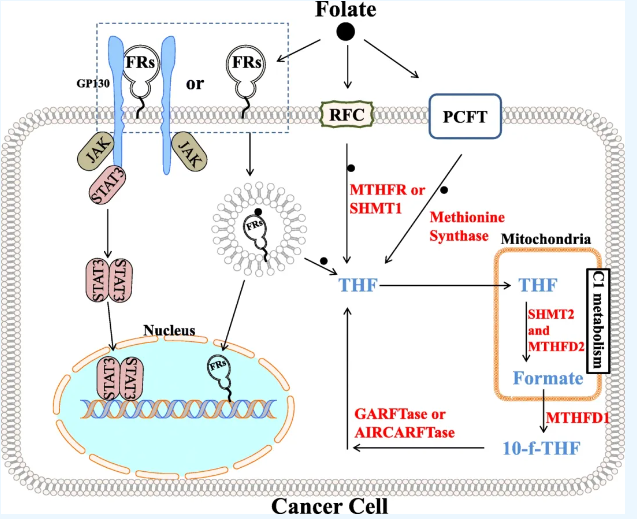
D1 Č~ËáĘÜķwĐÅĖēÍC1´úÖx
FRα
Č~ËáĘÜķwαŖ¨Folate receptor alphaŖŦFRαŖŠŌ˛ˇQé FOLR1ģōČ~ËáŊYēĪĩ°°×ŖŦŲĶÚ¸ßĶHēÍÁĻFRsŧŌ×åŖŦĘĮŌģˇN38-40 kDaĩÄĖĮģųÁ×ÖŦõŖŧĄ´ŧ(GPI)å^ļ¨ĩÄŧ°ûąíÃæĖĮĩ°°×ĄŖĶÉFOLR1ž´aŖŦĶÉ7Íâī@×ĶēÍ6ČēŦ×ĶŊMŗÉĄŖFRα°üēŦļāŊYĶōŖŦ°üĀ¨Č~ËáŊYēĪÎģücēÍGPIå^ļ¨ÎģücŖŦēķÕßØØĸFRαšĖļ¨ÔÚŧ°ûĤÉĪĄŖ
FRαĶĐļāˇNšĻÄÜĖØücŖē
ĸŲČ~ËáŪDß\ŖēFRαͨß^ŊYēĪČ~Ëá˛ĸŊé§ÆäČÍĖ×÷ĶÃŖŦĸČ~ËáŪDß\ßMŧ°ûŖģ
ĸÚÄ[ÁöÔöÖŗÕ{ŋØŖēFRαÔÚÄŗĐŠŋėËŲÔöÖŗĩÄ°Šŧ°ûÖĐąíß_ËŽÆŊÃ÷ī@ÔöŧĶŖŦŌōéß@ĐŠŧ°ûĐčŌĒ¸üļāĩÄČ~ËáížSŗÖÆäŽŗŖ¸ßĩÄÔöÖŗËŲÂĘēÍ´úÖxģîĐÔŖģ
ĸÛĐÅĖ÷§ŖēFRα
ĸÅcÄ[ÁöĩÄŊūĄĸŪDŌÆĄĸßMÕšŖŦ˛ĸͨß^ļāˇNCÖÆ
ĸÅcŧ°ûĐÅĖ÷§ŖŦČįͨß^GP130š˛ĘÜķwŊé§ĩÄJAKŌĀŲĐÔß^ŗĖŧ¤ģîSTAT3ŖŦģōÅcLYNĀŌ°ąËáŧ¤Ã¸ĐÎŗÉÍēĪÎīíÕ{šPEAK1ĩÄÁ×Ëáģ¯Ŗģ
ĸÜŪDäŌō×ĶŖēGPIå^ļ¨ĩÄFRαÔÚČģ¯ēķŋÉŌÔŪDŌÆĩŊŧ°ûēËŖŦ˛ĸÖąŊĶ×÷éŪDäŌō×Ķ°l]×÷ĶÃĄŖ
FRαÔÚļāˇNˇĮēĐÔŊMŋÖĐĶĐąíß_ŖŦĩĢÔÚÄŗĐŠķwÁöÖĐVˇē¸ßąíß_ŖŦČįÂŅŗ˛°ŠĄĸˇÎ°ŠĄĸŊYÄc°ŠēÍČéĪŲ°ŠĩČĄŖ¸ßß_90%ĩÄÂŅŗ˛°ŠŊMŗÉĐÔąíß_FRαŖŦļøÆäÔÚˇĮēĐÔÂŅŗ˛ŊMŋÖĐ×ēõ˛ģąíß_ŖģÔÚ76-89%ĩÄÉĪƤĐÔÂŅŗ˛°ŠÖĐß^ąíß_ŖģÔÚ14-74%ĩġĮĐĄŧ°ûˇÎ°ŠÖĐß^ąíß_ĄŖ
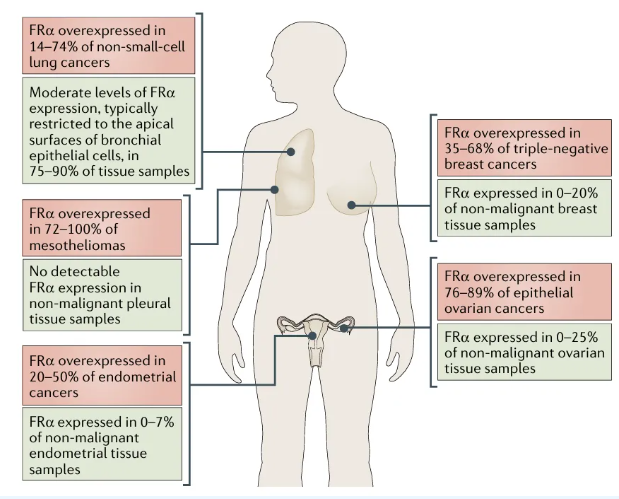
D2 ÔÚ°Š°Yē͡ĮēĐÔŊMŋÖĐFRαß^ąíß_Įér
FRαÄ[ÁöËÎīé_°lĮér
FRαķwÔÚÅßĖĨ°lÉúēķĩġĮēĐÔŊMŋÖĐžßĶĐ×îĐĄĩÄÉúĀí×÷ĶÃŖŦ˛ĸĮŌÔÚļāˇN°Š°YîĐÍÖĐß^ąíß_ŖŦĻˇĮÉúĀíĩ×Îī(ČįČ~Ëá)Ō˛žßĶиßËŽÆŊĩÄĶHēÍÁĻŖŦÍŦrŌ˛
ĸÅcÄ[ÁöĩÄŊūēÍŪDŌÆĄŖŌō´ËŖŦFRαŌŅŗÉéÄ[ÁöÖίÖĐ°Š°YŗÉĪņŖŦŌÔŧ°ŋšķwËĄĸADCĄĸĐĄˇÖ×ĶËÎīĄĸëpĖØŽĐÔŋšķwĄĸCAR-TĩČļāˇNÖίĘÖļÎĩÄĶĐЧ°ĐücĄŖ
ËĶēÍŗÉĪņ°ĐücŖēFRαŌ˛ĘĮĐãĩÄÄ[Áö°ĐĪōËĶēÍŗÉĪņ°ĐücĄŖĀũČįFolate-FITCŖŦŌ˛ˇQéEC17ŖŦĘĮŌģˇNČ~ËáĐŪīĩÄÉšâËĶˇÖ×ĶŖŦͨß^ĸÉšâËØŽÁōĮčËáû}Ŗ¨FITCŖŠÅcČ~ËáŊYēĪŖŦĀûĶÃČ~ËáĘÜķwŖ¨Folate ReceptorŖŦFRŖŠÔÚÄŗĐŠ°Šŧ°ûîĐÍÖĐĩÄß^ąíß_ŋÉŌÔÔöĻÄ[ÁöŊMŋĩÄŋÉŌģ¯ŖŦąČČįÔÚÂŅŗ˛°ŠĘÖĐgÖĐÍÖú×ReŪDŌÆĐÔ˛Ą×ĄŖ
ÎŋšËŖēFarletuzumab ͨß^ÅcFRαŊYēĪ°l]×÷ĶÃŖēĸŲŋšķwŌĀŲĐÔĩÄŧ°ûŊé§ĩÄŧ°ûļž×÷ĶÃŖ¨ADCCŖŠŖēŋÉŌÔÕT§ÃâŌßŧ°ûŖ¨Čį×ÔČģĸûŧ°ûŖŠšĨôēÍĸËĀąíß_ FRαĩÄÄ[Áöŧ°ûŖģĸÚŅaķwŌĀŲĐÔŧ°ûļžĐÔŖ¨CDCŖŠŖēŧ¤ģîŅaķwĪĩŊyŖŦ§ÖÂÄ[Áöŧ°ûĩÄÆÆÄŖģĸÛ´ŲßMÄ[Áöŧ°û×ÔĘÉŖēFarletuzumabÄÜōÕT§Ä[Áöŧ°û°lÉú×ÔĘÉŖŦß@ĘĮŌģˇNŧ°û×ÔÎŌĪûģ¯ĩÄß^ŗĖŖŦŋÉŌÔ§ÖÂŧ°ûšĻÄÜÕĪĩKēÍËĀÍöĄŖÔÚÅR´˛ÔōÖĐŖŦFarletuzumab ×÷éÎŌģËÎīģōÅcÆäËûģ¯¯ËÎīÂēĪĘšĶÃrŖŦŌŅŊī@ĘžŗöĻ FRαęĐÔ°Š°YģŧÕßĩÄÔÚ¯Đ§ĄŖ
ADCËÎīŖēADCËÎīElahereĶÉŌģáĻFRαĩÄŋšķwēÍŌģÎĸšÜŌÖÖÆŠDM4ŊMŗÉŖŦĘĮĘ׹ģÅúĘĶÃĶÚÂŅŗ˛°ŠĩÄŋšķwËÎīÅŧÂÎīĄŖÅR´˛Į°ŅĐžŋąíÃ÷ŖŦÔËÎīÔÚÂŅŗ˛°Šē͡ĮĐĄŧ°ûˇÎ°ŠÄŖĐÍÖĐžßĶĐķwÍâēÍķwČŋšÄ[ÁöģîĐÔĄŖElahereÅcÆäËûĶÃĶÚÂŅŗ˛°ŠģŧÕßĩÄËÎī(ČįØˇĨÎŋšĄĸ°ĸÚËØēÍŋ¨ãK)ÂēĪĘšĶÃĩÄÅR´˛Į°ķwČŅĐžŋŌ˛ī@ĘžŗöŋšÔöÖŗ×÷ĶÃĄŖ2024Äę3ÔÂ22ČÕŖŦFDAŌŅÅúĘELAHEREĶÃĶÚÖίĖØļ¨ÂŅŗ˛°ŠģŧÕߥŖ
CAR-TŖēēŦĶĐFRαĖØŽĐÔscFv (MOv19)ÅcTŧ°ûĘÜķwæCD3ζŊYēĪŖŦ˛ĸŊYēĪCD137 (4-1BB)š˛´Ėŧ¤ģųĐōĩÄš¤ŗĖģ¯CAR - Tŧ°ûŖŦÔÚÅR´˛Į°ÄŖĐÍÖĐŗÉšĻÕT§Ä[ÁöĪûÍËĄŖ´ËîCAR - Tŧ°ûÕũÔÚIÆÚÔōÖĐßMĐĐyÔĄŖEC17ŌŅąģĶÃĶÚÔušĀCAR-Tŧ°û¯ˇ¨ÖĐŖŦͨß^Č~ËáĘÜķwŊé§ĩÄëpĖØŽĐÔßmÅä×ĶˇÖ×ĶŖ¨bispecific adaptor molecule, CAMŖŠŋØÖÆĩÄCAR-Tŧ°ûĩÄģîĐÔĄŖ
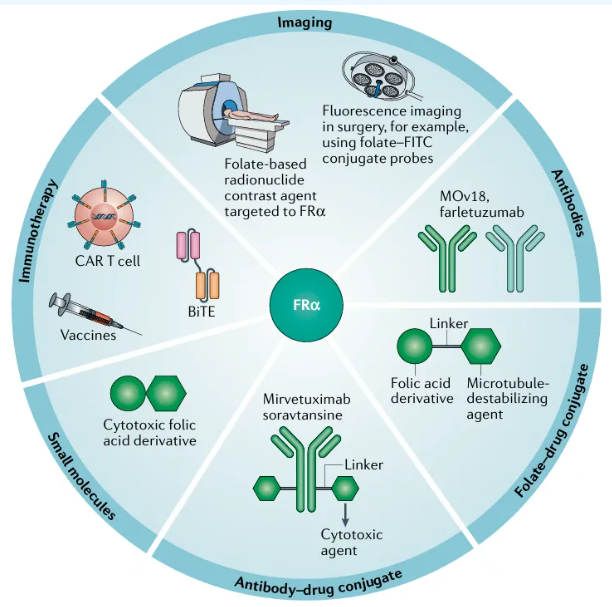
D3 FRα°ĐĪōËÎīÔÚ°Š°YÔ\āēÍÖίÖĐĩÄÅR´˛ĒĶÃĄŖ
FRαÔÚ°Š°YÖίÖĐĘĮŌģ¸ßļČĪāęPĮŌžßĶĐÔÚé_°lrÖĩĩÄ°ĐücŖŦĮ°ž°VˇēŖŦ°üĀ¨ĐÂËé_°lĄĸÂēĪÖί˛ßÂÔĄĸĐÔģ¯át¯ŌÔŧ°ĘĐöÁĻĩČĄŖëSÖøŅĐžŋĩÄÉîČëŖŦFRα°ĐĪōÖίĶĐÍûé°Š°YģŧÕßĖᚊ¸üļāĩÄÖίßxņē͸üēÃĩÄÖÎ¯Đ§šûĄŖ
S-RMab®ÎŋËÂĄŋšķw
Ëšß_ĖØÉúÎīŌŅÉĪŧÜFRαÍÃÎŋšŖŦžßĶиü¸ßĩÄĖØŽĐÔĄĸė`ÃôļČĄĸˇļ¨ĐÔŖŦéÅR´˛Ėᚊ¸üĘ´_ĩÄÔ\āŊYšûĄŖ
ĸŋŧÎÄĢI
[1] Scaranti M, Cojocaru E, Banerjee S, Banerji U. Exploiting the folate receptor α in oncology. Nat Rev Clin Oncol. 2020 Jun;17(6):349-359.
- Č~ËáĘÜķwĻÁĩÄšĻÄÜŧ°ÔÚ°Š°YÖί˛ßÂÔÖĐĩÄļāÃæĐÔĒĶÃ
- HbA1cÅäĻŋšķwÔÚĖĮÄō˛ĄŅĐžŋÅcÅR´˛Ô\āÖĐĩÄĒĶÃŨ
- CD45ĩÄÉúÎīWšĻÄÜŧ°×÷é°ĐücÔÚÃâŌßÖίÖĐĩÄĒĶÃÁĻ
- p16/Ki-67ëpČžzyÔÚ×Ķmîi°ŠĮ°˛Ą×Ô\āÖĐĩÄŨ
- ŌüS´ŧŊYēĪĩ°°×4Ŗ¨RBP4ŖŠŋšķwÔÚļāˇNŧ˛˛ĄīLëUÖĐĩÄÔ\āŧ°ĒĶÃÁĻ
- ŋÉČÜĐÔfmsĶĀŌ°ąËáŧ¤Ã¸-1(sFlt-1)ĻČŅÉīĪČÕ××Ķ°BĩÄĶ°íŧ°Ô\ārÖĩ
- ĶÄéTÂŨĐũUžú(Hp)ĩÄzyˇŊˇ¨ŧ°ÖØŊMÍÃÎŋšÍÆË]
- ĐÂÅd°ĐücB7-H3ĄĸB7-H4ŋįĤĩ°°×ĩÄ×÷ĶÃŧ°ÔÚADCËÎīŅĐ°lÖĐĩÄĒĶÃ
- Ëšß_ĖØÉúÎīĸÁÁĪā2025ÄęÃĀøAACRÕšūŖŦÕ\ŅûÄúÉWÅRŖĄ
- MCEÖą˛ĨîA¸æŖēã~ËĀÍöĩÄCÖÆĖŊË÷ÅcátWĒĶÃ
- 2024ĩÚžÅÃŌßÃįÖĐøîI§ÕßÄęūͨÖĒ
- MCEÍÆŗöŗŦ900ˇNŌģŋšēÍļāˇNļūŋšŽaÆˇŖŦēÉwáéT°Đüc
- ĩ¤ŧ{ēÕĸĘÕŲAbcamŌÔÍÆĶÉúÃüŋÆWîIĶōŅĐžŋĐÂßMŗĖ
- îŖŊŨÉúÎīĐÂWÆÚиŖĀûŖŦËÄÖØģŨĪŪrĪí
- °ÛÖZČĢž°ŋÆŅĐmIHC˛ĄĀíŧŧĐgˇūÕÄęÖĐ´ķ´ŲäNģđáíŌu
- Î÷ÃĀŊÜKPLáäNļūŋšēÍĩ×ÎīĪŪrģŨģîĶŌŅĸĶŖĄ





