抗體-藥物偶聯物(ADC)內化效率檢測原理、步驟及優勢
ADC內化效率檢測原理
DT3C(Diphtheria Toxin Fragment A and Streptococcus Protein G C1, C2, C3)是一種重組表達的融合蛋白,由白喉毒素的Fragment A(僅毒素部分)和G群鏈球菌的3C片段(IgG結合部分)融合而成。該蛋白能夠與抗體的Fc端高度親和,與抗體結合的DT3C分子在抗體被內吞時一同進入細胞。DT3C可以與任何IgG型抗體結合,因此可用于檢測來自不同物種的抗體內化效率。DT3C與抗體結合后形成的mAb-DT3C偶聯物在體外模擬ADC藥物的作用機制,有助于在藥物研發早期階段評估抗體的內化能力和藥物的釋放效率。
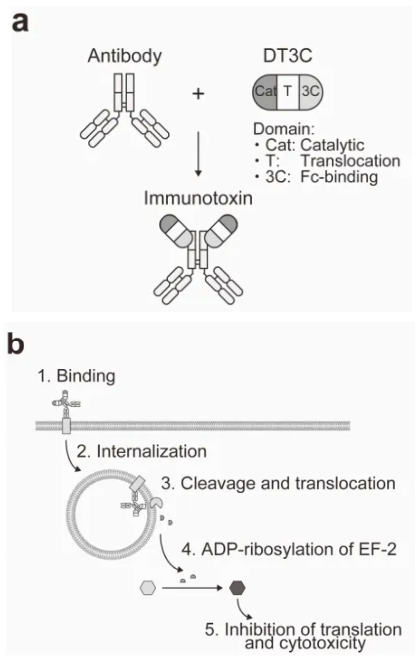
(a) DT3C由催化(Cat)、轉位(T)和Fc結合(3C)結構域組成。DT3C的Fc結合結構域特異性地與抗體結合。
(b) mAb-DT3C偶聯復合物識別并結合細胞表面抗原后,mAb-DT3C-抗原復合物被內化。,其中DT3C的轉位末端被細胞弗林蛋白酶切割,DT3C的催化結構域被釋放到細胞質中,DT3C釋放出具有毒性的DT,DT能夠抑制EF2-ADP核糖基化的活性,阻斷蛋白翻譯過程,最終導致細胞死亡。
未進入細胞的DT3C則不具有殺傷細胞的活性,因此可根據細胞殺傷情況來評價抗體的內化效率。
檢測步驟
01 制備mAb-DT3C偶聯物
將DT3C蛋白和目的抗體在室溫下孵育30分鐘,形成mAb-DT3C共軛物。
02 共培養
將mAb-DT3C偶聯物直接加到含有抗原陽性細胞(如腫瘤細胞)的完全培養基中進行孵育。
03 檢測內化效率
通過流式細胞術或熒光顯微鏡等方法,檢測細胞活力或細胞死亡情況,從而評估抗體在細胞表面的內化效率。
DT3C檢測ADC藥物抗體內化效率優勢
廣泛適用性:可與來自不同物種(如人、小鼠、兔、山羊)的任何IgG結合。
高效性:在室溫下孵育30分鐘即可形成mAb-DT3C偶聯物。DT3C在細胞內能夠迅速釋放出具有毒性的DT,從而快速評估抗體的內化效率。
內化效率高:分子量小于Mab-ZAP,mAb-DT3C內化效率高于mAb-Mab-ZAP。
便捷性:通過流式細胞術或熒光顯微鏡等方法,即可快速、準確地檢測mAb在細胞表面的內化效率。
注意事項:在進行體外檢測時,應確保實驗條件的一致性,如細胞種類、細胞濃度、DT3C和抗體的比例、孵育時間等。需要嚴格控制實驗過程中的無菌操作,以避免外界因素的干擾。
展望
隨著生物制藥技術的不斷發展,ADC藥物在腫瘤治療中的應用前景日益廣闊。然而,ADC藥物的療效受多種因素影響,其中抗體的內化效率是關鍵因素之一。因此,對抗體內化效率的準確評估對于ADC藥物的研發具有重要意義。DT3C重組蛋白作為一種高效、簡便、廣泛適用的評價工具,將在ADC藥物研發中發揮越來越重要的作用。未來,隨著DT3C技術的不斷完善和應用領域的拓展,相信將為ADC藥物的研發提供更多有力的支持。
Starter提供高純度的DT3C蛋白,助力ADC藥物研發
DT3C (Diphtheria toxin & spg 3C domain) Protein, Corynephage beta
貨號:UA070063
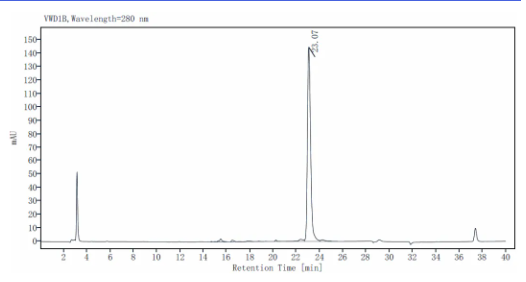
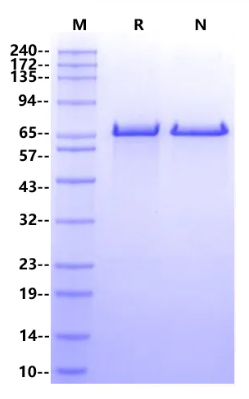
>90% by SDS-PAGE and HPLC
產品信息
杭州斯達特(www.starter-bio.com)志在為全球生命科學行業提供優質的抗體、蛋白、試劑盒等產品及研發服務。依托多個開發平臺:重組兔單抗、重組鼠單抗、快速鼠單抗,重組蛋白開發平臺(E.coli,CHO,HEK293,Insect Cells),已正式通過歐盟98/79/EC認證、ISO9001認證ISO13485。





