揭秘TH17細(xì)胞分化“開關(guān)”:ChIP-seq 技術(shù)破解基因調(diào)控密碼
2017年發(fā)表在Nature上的“Reversing SKI–SMAD4-mediated suppression is essential for TH17 cell differentiation”的文章揭示了TGFβ的“反向調(diào)控”策略:正常情況下,SMAD4蛋白與抑制因子SKI形成復(fù)合物,像“基因剎車”一樣抑制TH17核心轉(zhuǎn)錄因子RORγt的表達(dá);而TGFβ通過誘導(dǎo)SKI降解,解除這一抑制,最終激活TH17分化程序。更重要的是,研究發(fā)現(xiàn)的SKI-SMAD4 信號軸,為靶向調(diào)控TH17細(xì)胞提供了全新治療靶點(diǎn)。該研究通過ChIP-seq技術(shù)發(fā)現(xiàn)SMAD4并非廣泛抑制TH17相關(guān)基因,而是特異性結(jié)合RORγt基因(Rorc)的啟動子區(qū)域,直接抑制其轉(zhuǎn)錄。

研究背景
TH17細(xì)胞在宿主防御、炎癥和自身免疫中至關(guān)重要,TGFβ與IL-6協(xié)同對TH17細(xì)胞分化起重要作用,但TGFβ促進(jìn)TH17細(xì)胞分化的機(jī)制尚不清楚。
技術(shù)路線
TH17細(xì)胞在宿主防御、炎癥和自身免疫中至關(guān)重要,TGFβ與IL-6協(xié)同對TH17細(xì)胞分化起重要作用,但TGFβ促進(jìn)TH17細(xì)胞分化的機(jī)制尚不清楚。
技術(shù)路線
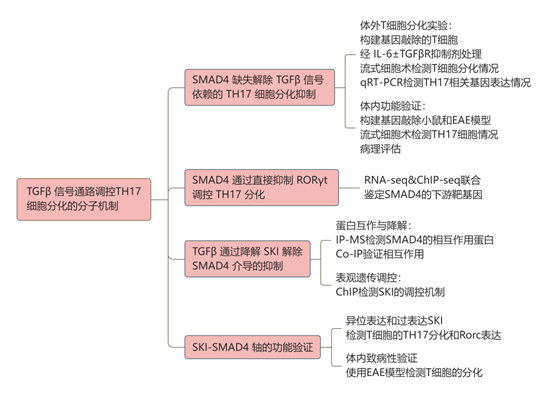
研究結(jié)果
本研究首先通過體外分化實(shí)驗(yàn)發(fā)現(xiàn)SMAD4缺失的T細(xì)胞在僅含IL-6、無TGFβ信號時(shí),仍能高效分化為TH17細(xì)胞,而野生型T細(xì)胞無法分化;雙敲除小鼠(同時(shí)缺失SMAD4和TGFβRII)的T細(xì)胞在IL-6單刺激下,TH17相關(guān)基因(Rorc、Il17a、Il23r等)表達(dá)顯著上調(diào),與SMAD4缺失的T細(xì)胞結(jié)果一致。進(jìn)而又進(jìn)行了體內(nèi)功能驗(yàn)證,結(jié)果顯示雙敲除小鼠脾臟和淋巴結(jié)中TH17細(xì)胞比例與野生型相當(dāng),而單純TGFβRII敲除小鼠幾乎無TH17細(xì)胞。在實(shí)驗(yàn)性自身免疫性腦脊髓炎(EAE)模型中,雙敲除的T細(xì)胞分化為致病性TH17細(xì)胞的能力與野生型一致,且小鼠表現(xiàn)出類似的病理損傷。誘導(dǎo)型SMAD4缺失實(shí)驗(yàn)顯示,急性缺失 SMAD4可在無TGFβ受體信號時(shí)促進(jìn)TH17分化,證實(shí)SMAD4是抑制TH17分化的關(guān)鍵分子。以上結(jié)果表明SMAD4缺失解除TGFβ信號依賴的TH17細(xì)胞分化抑制。
本研究首先通過體外分化實(shí)驗(yàn)發(fā)現(xiàn)SMAD4缺失的T細(xì)胞在僅含IL-6、無TGFβ信號時(shí),仍能高效分化為TH17細(xì)胞,而野生型T細(xì)胞無法分化;雙敲除小鼠(同時(shí)缺失SMAD4和TGFβRII)的T細(xì)胞在IL-6單刺激下,TH17相關(guān)基因(Rorc、Il17a、Il23r等)表達(dá)顯著上調(diào),與SMAD4缺失的T細(xì)胞結(jié)果一致。進(jìn)而又進(jìn)行了體內(nèi)功能驗(yàn)證,結(jié)果顯示雙敲除小鼠脾臟和淋巴結(jié)中TH17細(xì)胞比例與野生型相當(dāng),而單純TGFβRII敲除小鼠幾乎無TH17細(xì)胞。在實(shí)驗(yàn)性自身免疫性腦脊髓炎(EAE)模型中,雙敲除的T細(xì)胞分化為致病性TH17細(xì)胞的能力與野生型一致,且小鼠表現(xiàn)出類似的病理損傷。誘導(dǎo)型SMAD4缺失實(shí)驗(yàn)顯示,急性缺失 SMAD4可在無TGFβ受體信號時(shí)促進(jìn)TH17分化,證實(shí)SMAD4是抑制TH17分化的關(guān)鍵分子。以上結(jié)果表明SMAD4缺失解除TGFβ信號依賴的TH17細(xì)胞分化抑制。
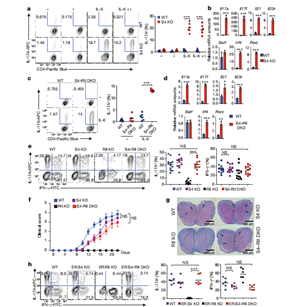
圖1. SMAD4缺失導(dǎo)致在缺乏TGFβ信號的情況下TH17細(xì)胞分化。
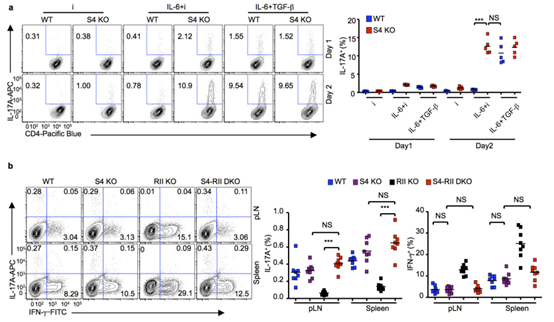
圖S1. 在沒有SMAD4的情況下TH17細(xì)胞分化。
接下來作者對SMAD4缺失如何影響控制TH 17細(xì)胞分化的分子機(jī)制進(jìn)行了研究。利用RNA-seq檢測基因表達(dá)差異,結(jié)果顯示SMAD4缺失的T細(xì)胞激活后12h內(nèi),Rorc表達(dá)顯著升高,早于其他TH17相關(guān)基因(如Il17a、Batf),且RORγt蛋白水平同步上調(diào)。回補(bǔ)SMAD4可抑制SMAD4缺失的T細(xì)胞Rorc表達(dá)及 TH17分化,而異位表達(dá)RORγt可逆轉(zhuǎn)SMAD4的抑制作用,證實(shí)了RORγt是SMAD4的關(guān)鍵下游靶點(diǎn)。并通過ChIP-seq 進(jìn)行了驗(yàn)證,結(jié)果顯示SMAD4直接結(jié)合Rorc基因的啟動子和增強(qiáng)子區(qū)域,但不結(jié)合Il17a/Il17f。以上結(jié)果表明SMAD4 通過直接抑制RORγt調(diào)控TH17分化。
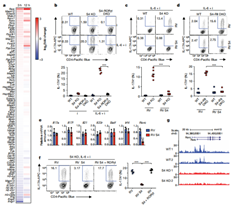
圖2. SMAD4通過直接抑制Rorc表達(dá)來控制TH17細(xì)胞程序。
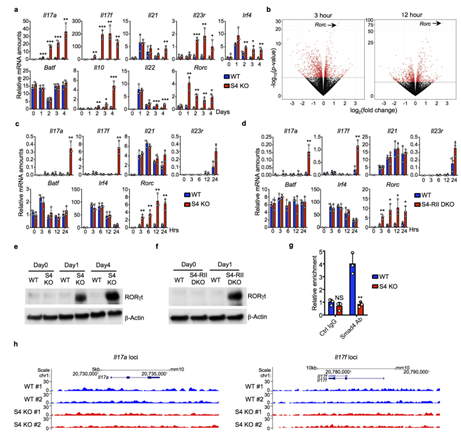
圖S2. SMAD4抑制RORγt表達(dá)。

圖S2. SMAD4抑制RORγt表達(dá)。
以上研究中發(fā)現(xiàn)無論是否存在TGFβ,SMAD4仍然與Rorc位點(diǎn)結(jié)合,作者提出TGFβ信號通路改變了SMAD4與其他蛋白質(zhì)的相互作用的假設(shè)。通過IP-MS和Co-IP發(fā)現(xiàn),SMAD4與轉(zhuǎn)錄抑制因子SKI結(jié)合,且TGFβ刺激可顯著降低SKI蛋白水平,破壞SKI-SMAD4復(fù)合物;SMAD4突變體(無法結(jié)合SKI)失去對TH17分化的抑制能力,證實(shí)了SKI-SMAD4互作是抑制RORγt的關(guān)鍵。接著對SKI的調(diào)控機(jī)制進(jìn)行了研究,發(fā)現(xiàn)SKI過表達(dá)可抑制Rorc啟動子區(qū)H3K9乙酰化,而SMAD4缺失可逆轉(zhuǎn)這一效應(yīng),表明SKI-SMAD4復(fù)合物通過調(diào)控染色質(zhì)修飾抑制基因表達(dá)。經(jīng)TGFβ處理的野生型T細(xì)胞,Rorc啟動子H3K9乙酰化水平升高,而SMAD4缺失的T細(xì)胞在無TGFβ時(shí)仍維持高乙酰化,進(jìn)一步證明了TGFβ通過降解SKI解除去乙酰化抑制。以上結(jié)果表明,TGFβ通過降解SKI解除SMAD4介導(dǎo)的抑制。
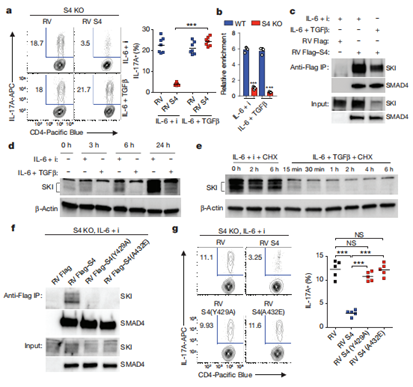
圖3. TGFβ信號破壞SKI-SMAD4復(fù)合物,以促進(jìn)TH17細(xì)胞分化。
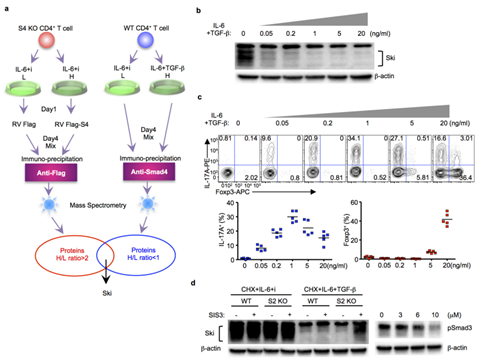
S3. 低劑量TGFβ下SKI的鑒定及其降解。
最后作者對SKI-SMAD4軸的功能進(jìn)行了驗(yàn)證。異位表達(dá)SKI可顯著抑制野生型T細(xì)胞的TH17 分化和Rorc表達(dá),且該抑制作用依賴SMAD4;干擾SKI表達(dá)可使野生型T細(xì)胞在無TGFβ時(shí)分化為TH17細(xì)胞,證明了SKI是TH17分化的負(fù)調(diào)控因子。體內(nèi)致病性結(jié)果顯示,過表達(dá)SKI的T細(xì)胞在EAE模型中分化為TH17細(xì)胞的能力顯著受損,而SKI缺陷細(xì)胞分化增強(qiáng),表明SKI-SMAD4 軸在體內(nèi)調(diào)控TH17細(xì)胞的致病性分化。
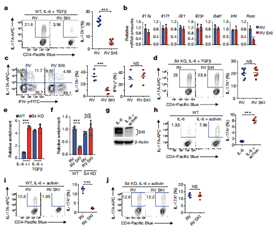
圖4. SKI以SMAD4依賴的方式抑制TH17細(xì)胞分化。
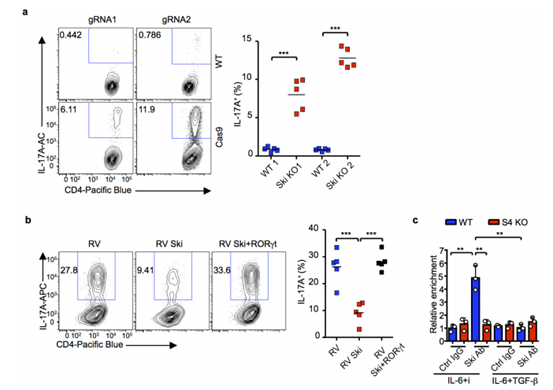
圖S4. SKI和SMAD4協(xié)同抑制TH17細(xì)胞分化。
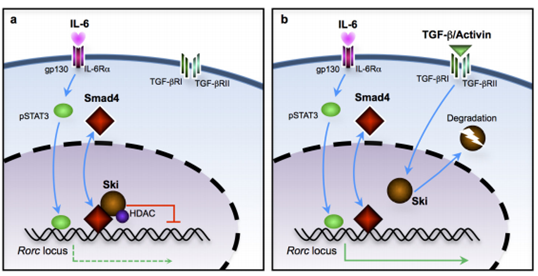
圖S5. TGFβ超家族信號克服了激活T細(xì)胞中SKI-SMAD4復(fù)合物介導(dǎo)的RORγt表達(dá)抑制,以促進(jìn)TH17細(xì)胞分化。
本研究通過基因敲除、分子互作、表觀遺傳及體內(nèi)外功能實(shí)驗(yàn),系統(tǒng)性闡明了TGFβ-SKI-SMAD4-RORγt通路在TH17細(xì)胞分化中的關(guān)鍵機(jī)制,為靶向SKI-SMAD4軸治療TH17相關(guān)疾病(如自身免疫病)提供理論依據(jù)。
標(biāo)簽:
ChIP-seq
染色質(zhì)免疫共沉淀測序
- 揭秘TH17細(xì)胞分化“開關(guān)”:ChIP-seq 技術(shù)破解基因調(diào)控密碼
- DAP-seq技術(shù)助力揭秘葡萄耐冷性的糖代謝調(diào)控機(jī)制
- DAP-seq技術(shù)助力揭示擬南芥根基本組織發(fā)育的調(diào)控機(jī)制
- 客戶文章(Plant Com) DAP-seq助力揭示甘藍(lán)型油菜早花的遺傳機(jī)制
- 利用建庫篩選與單細(xì)胞測序技術(shù)對CAR信號模塊搭建進(jìn)行研究
- Ribo-seq技術(shù)原理與應(yīng)用方向
- RBP研究技術(shù)RIP-seq+Polysome profiling
- Cell文獻(xiàn):轉(zhuǎn)座子外顯化構(gòu)成了一個(gè)受進(jìn)化選擇的功能蛋白質(zhì)亞型儲庫
Copyright(C) 1998-2025 生物器材網(wǎng) 電話:021-64166852;13621656896 E-mail:info@bio-equip.com





