C9orf72相關FTD和ALS的腦脊液生物標記物分析方法介紹
C9orf72 基因中的GGGGCC重復擴增是額顳葉癡呆(FTD)和肌萎縮側索硬化(ALS)最常見的遺傳原因,而且重復的非ATG翻譯導致二肽重復蛋白(DPRs)的產生。隨著靶向重復擴增的潛在療法進入臨床試驗,迫切需要一種高敏的生物標記物對靶點作用進行分析。本文研究者利用Simoa技術開發了一種靈敏可靠的poly(GP)二肽重復蛋白測定方法。

文章題目:Development of a sensitive trial-ready poly(GP) CSF biomarker assay for C9orf72-associated frontotemporal dementia and amyotrophic lateral sclerosis
發表時間:2022年4月
期刊名稱:J Neurol Neurosurg Psychiatry
影響因子:13.654
DOI:10.1136/jnnp-2021-328710
研究概述
研究人員通過Simoa平臺開發了一種免疫分析方法,用于測量C9orf72相關FTD和ALS患者腦脊液(CSF)中C9orf72重復擴增產生的poly(GP) 二肽重復蛋白(DPR)。
研究表明,該分析方法高度靈敏和穩定,通過了廣泛的鑒定標準,板內、板間的變異性低、標曲和樣品的精密度和準確度高、稀釋線性好、對樣品和標準凍融具有耐受性,以及不受血紅蛋白干擾。使用這種方法來測量FTD突變攜帶者隊列收集的CSF樣本中的poly(GP) (N=40 C9orf72和15個對照)。CSF中C9orf72的poly(GP) 信號,樣本組的平均信號值比對照組高38倍,最低的樣本比對照組高8倍,均低于該方法的定量下限。而且檢測的特異性和敏感性均為100%,靶標檢測的窗口較大。
這些數據表明,基于Simoa的poly(GP)DPR分析適合用于臨床試驗,以明確旨在減少C9orf72重復的治療藥物的靶向治療。
研究內容
1、Simoa poly(GP) assay建立
首先使用Simoa HD-1對assay進行優化。研究人員測試了一系列抗體,包括小鼠抗GP單克隆抗體(mGP),和一系列針對不同長度GP肽的兔多克隆抗體(GP57、GP60和GP6834)。綜合考慮后選擇了小鼠抗GP單克隆抗體(mGP)作為捕獲抗體,多克隆抗體組合(GP57−60)作為檢測抗體,標準品為GST-GP32肽段。這套組合的信噪比最高,為2.51;且LLOQ最低,為1.04pg/ml(圖1)。為了確保長期的兼容性,接下來將分析轉移到新的Simoa HD-X平臺。且對該assay進行了重新優化,將標準曲線稀釋液從裂解液稀釋液B(HD-1)更改為稀釋液A(HD-X)效果最好(圖2A)。此外,SBG從100μM降至50μM,LLOQ為1.17 pg/mL(圖2B)。
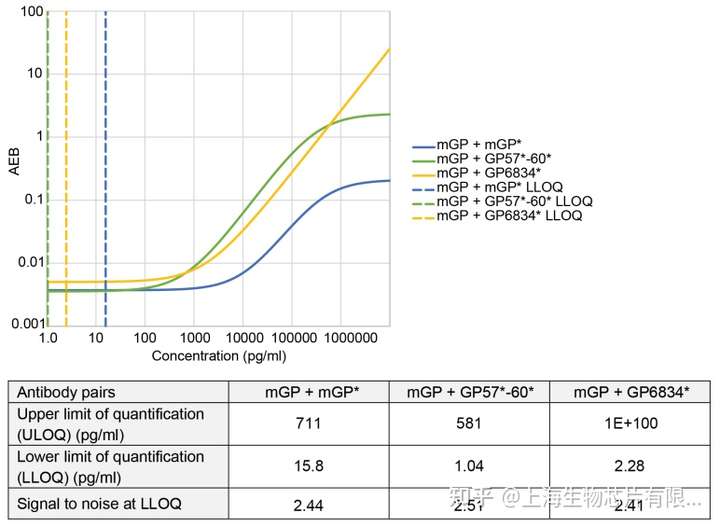
Fig.1 Simoa homebrew assay中各抗體組合的比較。虛線分別表示每種測定方法優化后預測的LLOQ。AEB:平均每顆磁珠上的酶標數;LLOQ:定量下限;Simoa:單分子陣列;*:代表此種抗體已標記上生物素。
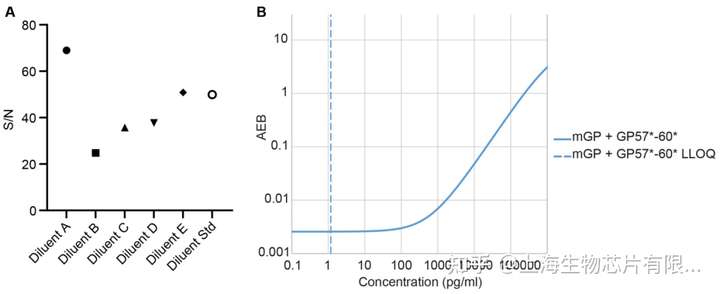
Fig.2 將poly(GP) assay轉移到Simoa HD-X平臺。(A)在人腦脊液加入25 pg/mL GST-GP32標準品,然后用不同的Quanterix稀釋液1:2進行稀釋,通過比較信號/噪聲(S/N)來評估樣品稀釋液的效果。(B)使用Quanterix分析顯像工具計算擬合的標準品曲線,虛線顯示LLOQ為1.17 pg/mL。
2. Simoa poly(GP) assay驗證為將該assay用于臨床試驗,使用標準生物標記物分析鑒定標準進行評估(表2)。由圖3可知,各項結果表明,該測定具有高度的靈敏度和穩健性,通過了標準生物標記物分析鑒定標準的評估,包括板內和板間的低變異性、標準品和樣品的高精密度和準確度、稀釋線性、樣品和標準凍融耐受性以及血紅蛋白干擾測試。
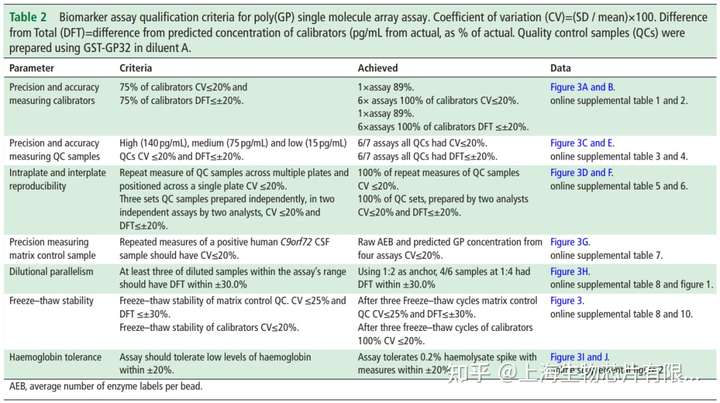
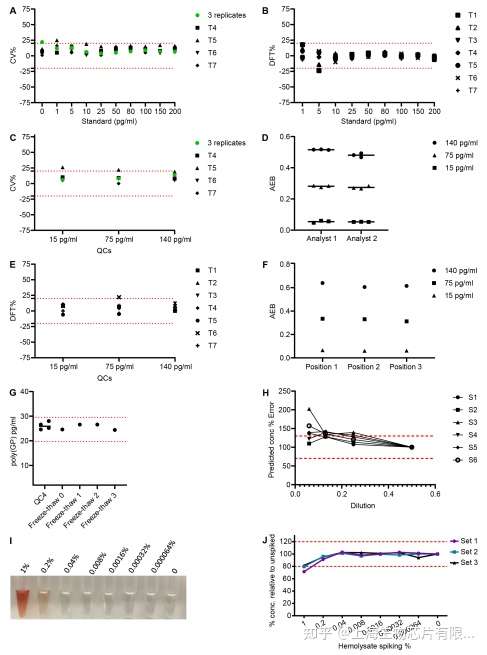
Fig.3 CSF poly(GP) Simoa assay驗證結果。制備了10點標準曲線和3個質量控制(QC)樣品,分別進行了7次獨立檢測。(A) 每個標準品的變異系數(CV)均小于20%。(B)每個標準品的總差(DFT)。DFT=標準品的預測濃度與實際濃度之差的%。(C)QC樣品的CVs。(D)由兩個工作人員分別制備的QC樣本的AEB信號值。(E) QC樣品
3.使用優化的Simoa測定法測量C9orf72 擴增載體CSF中的poly(GP)
使用這種優化后的測定方法來測量健康對照組(N=15)和C9orf72擴增陽性組(N=40)的腦脊液隊列中的poly(GP)。來自最低C9orf72樣本的分析信號的信噪比是對照樣本平均信號的八倍,顯示出與對照CSF信號的明顯分離(圖4A)。C9orf72組與對照組的信噪比平均為38倍。健康人腦脊液中的poly(GP)在15個樣本中有13個低于檢測限,其余2個低于LLOQ。
在所有C9orf72組中檢測到poly(GP)高于LLOQ,在沒有健康對照的情況下,敏感性和特異性均為100%。在C9orf72擴增陽性樣本中,poly(GP) 的測量范圍為6-148 pg/mL。發現男性和女性C9orf72擴增陽性樣本之間的poly(GP) 水平沒有差異。發現CSF poly(GP)水平與癥狀性C9orf72擴增陽性樣本(n=15)的發病年齡之間沒有相關性(圖4C)。有趣的是,對所有40例C9orf72擴增陽性病例進行分析后發現,樣本采集時的年齡與腦脊液中測得的poly(GP)之間存在顯著的中度正相關(r=0.3643)。然而,如果從分析中刪除具有最高poly(GP)水平的情況,則p值變為p=0.0522。
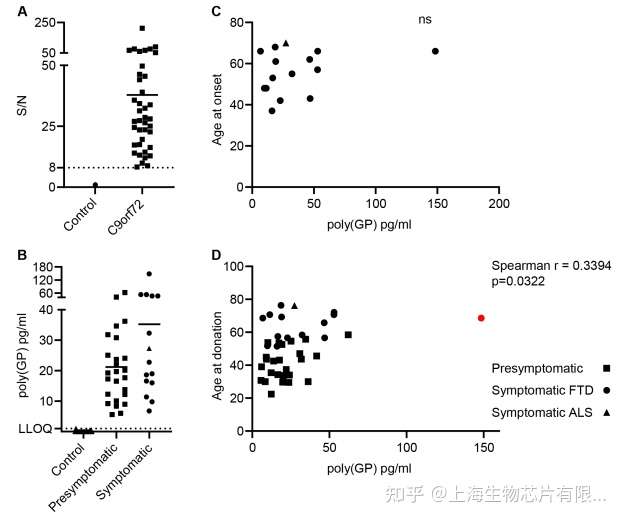
Fig.4 C9orf72擴增攜帶者腦脊液中Poly(GP) 水平
總結
- 準確測量FTD和ALS引起C9orf72 重復擴增產生的DPR,將是評估臨床試驗中重復/DPR降低策略目標參與度的關鍵工具。
- 現有免疫測定法,可以檢測患者CSF中的poly(GP) DPR,但由于一些患者的poly(GP) 水平接近背景,可能需要提高靈敏度。
- 該研究報告了一種適合臨床試驗的超靈敏腦脊液聚糖蛋白檢測方法的開發。能在絕大多數試驗參與者中評估目標參與度,包括低聚糖蛋白水平的參與者。
參考文獻:Wilson KM, Katona E, Glaria I, Carcolé M, Swift IJ, Sogorb-Esteve A, Heller C, Bouzigues A, Heslegrave AJ, Keshavan A, Knowles K, Patil S, Mohapatra S, Liu Y, Goyal J, Sanchez-Valle R, Laforce RJ, Synofzik M, Rowe JB, Finger E, Vandenberghe R, Butler CR, Gerhard A, Van Swieten JC, Seelaar H, Borroni B, Galimberti D, de Mendonça A, Masellis M, Tartaglia MC, Otto M, Graff C,Ducharme S, Schott JM, Malaspina A, Zetterberg H, Boyanapalli R, Rohrer JD, Isaacs AM; Genetic FTD Initiative (GENFI). Development of a sensitive trial-ready poly(GP) CSF biomarker assay forC9orf72-associated frontotemporal dementia and amyotrophic lateral sclerosis. J Neurol Neurosurg Psychiatry. 2022 Apr 4:jnnp-2021-328710. doi: 10.1136/jnnp-2021-328710. Epub ahead of print. PMID: 35379698.





