國自然研究熱點—eccDNA的前世今生
1. eccDNA為什么火?它到底是何方神圣?
2019年11月,頂尖國際學術期刊《Nature》和《Cell》相繼發表了關于染色體外環狀DNA(extrachromosomal circular DNA,eccDNA)的重要研究,徹底顛覆了人們對癌基因的傳統認知,同時也迅速引爆了整個生物醫學界,一時之間,將人們的目光都吸引到這個科研界的新寵兒身上。
其實,這種DNA并不是首次被發現,早在1965年就有關于eccDNA的報道,但當時并沒有引起科學界重視,認為它只是染色體外無意義的垃圾碎片。近年來研究表明,eccDNA往往在腫瘤和衰老過程中富集,以特殊的方式參與腫瘤和衰老的發生發展進程。在大部分人類癌癥細胞中eccDNA廣泛存在,且它的富集通常會促進癌基因的擴增,從而增加了癌基因的可塑性和不穩定性,因此其對腫瘤細胞的進化可能存在重要的意義,這一發現使eccDNA一躍成為科研界的新寵兒。
2. eccDNA的主要特征
(1) 長度特征
目前對eccDNA的大小還沒有定論,eccDNA大部分小于25kb,主要分布在0.1-5KB,但不同的文獻報道中表述略有差別。它們往往是一些特殊的基因區域形成的,可攜帶完整的基因和特殊的調控元件,能獨立完成復制過程,但不攜帶著絲粒和端粒結構。
(2) 結構特征
早期對eccDNA結構認識比較局限,主要發現它們是環狀DNA分子,并且往往是一些基因擴增的產物,其中也包含著DNA復制起始點,因此可以獨立完成復制作用。2019年,Nature以及Cell文章對eccDNA的結構有了較為深刻的探索分析,發現eccDNA不僅攜帶了完整的基因,還攜帶了基因上游的啟動子和增強子元件。eccDNA的染色質結構更加松散,其中的電鏡照片也清楚的顯示eccDNA為游離在染色體之外的環狀DNA分子。
(3) 形成特征
早期的研究發現eccDNA是基因擴增的產物,是基因組不穩定性的一種表現形式。腫瘤基因擴增往往以兩種方式,一種是在染色體上進行基因的擴增,另一種則是形成eccDNA。目前關于腫瘤中eccDNA的形成機制還沒有定論。早期的研究認為短重復序列是介導eccDNA形成的因素,主要通過基因重組機制實現,也有一些模型認為是在DNA復制過程中通過loop切除或在DNA復制暫停的時候復制泡中斷裂的DNA片段連接形成。2018年,Anindya Dutta等在他們的一篇綜述文章中用示意圖展示了各種可能形成eccDNA的分子模型。
(4) 表達特征
eccDNA可以攜帶完整的基因,尤其是腫瘤中經常攜帶致癌的驅動基因,不受控制的表達這些基因,最終導致腫瘤的惡性增長。eccDNA是基因擴增的一種形式,對癌基因的表達增高有重要的貢獻。早期的研究聚焦于發現eccDNA的存在,并且是癌基因擴增的重要形式,認為這對癌基因表達的貢獻主要是由于基因拷貝數的增加所致。2019年,Nature和Cell文章表明,eccDNA中染色質高度開放,并且其上存在著增強子序列,這些特征都提高了它的轉錄活性,因此,eccDNA對癌基因的過度表達既有拷貝數增加的因素,更有eccDNA本身高度轉錄活性的貢獻。
3. eccDNA的常見功能
早期人們一直認為eccDNA的存在是無意義的,直到2014年,Mischel實驗室發現膠質母細胞瘤對EGFR抑制劑的耐藥性是由eccDNA上的EGFRvIII功能獲得性突變的可逆性丟失引起的,人們才重新開始注意ecDNA的功能。檢測結果發現在天然染色體位點上的癌基因擴增相對較少,但是在癌癥中ecDNA的擴增則較為普遍。2017年,Kristen等人通過比較腫瘤基因組和生殖細胞基因組之間的序列,發現在天然染色體位點上的癌基因擴增相對較少,但是在癌癥中eccDNA的擴增則較為普遍。隨后,越來越多的實驗都表明,eccDNA的存在是強大且普遍的,它可以使癌基因在腫瘤細胞中的拷貝數大量增加,而這對于染色體擴增來說是很難實現的。
eccDNA不帶著絲粒元件,因此不能通過有絲分裂的方式均勻分配到分裂后的細胞中。但eccDNA可以通過不對稱分布,在腫瘤細胞中實現定向富集。尤其是攜帶了癌基因的腫瘤細胞,會因為癌基因拷貝數的增高而獲得生長速度的優勢,不對稱分裂過程中攜帶越多的eccDNA,細胞就會獲得越強的生存優勢,因此這種基于不對稱分布狀態的遺傳機制能在快速增殖的細胞中定向富集,因而其擴增使腫瘤能夠快速獲得并維持瘤內遺傳異質性,這也意味著eccDNA在加速腫瘤進化中起著核心作用。
eccDNA作為獨立的DNA分子,在細胞中發揮功能的方式和機制是非常重要的問題。目前對eccDNA的功能有一定的研究,但相信隨著研究的不斷深入,未來一定會有更多新的功能被發現。Anindya Dutta等在他們的綜述文章中系統的匯總了eccDNA的主要功能,如下圖。
4. eccDNA的研究思路
所謂兵馬未動,糧草先行!eccDNA的研究也是一場沒有硝煙的戰爭,須得搶占先機,方能知己知彼,百戰不殆。為了各位在這場“戰爭”中取得勝利,云序生物也為大家總結了eccDNA研究的思路。從文章的工作量、難易程度及雜志發表角度看,小編把eccDNA研究思路分為表達譜分析,生物標志物,功能機制研究三大類。那么接下來小編將從這三個角度給大家詳述。
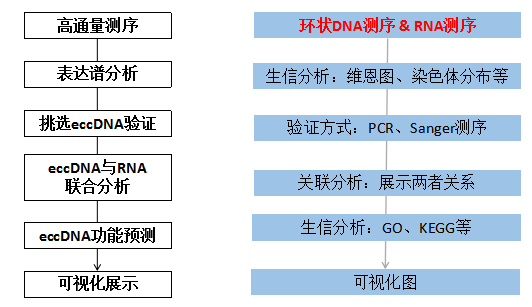
由于eccDNA屬于最新的研究分子,其在眾多物種和疾病中的分布情況都是未知的,這是研究eccDNA首先要解決的問題,也是各位科研工作者最好的一個切入點。不管研究什么內容,首先要做的就是確定好研究物種,疾病模型,樣品類型等基本信息。接下來,通過高通量手段即環狀DNA測序和RNA測序(云序生物提供此服務),確定eccDNA在樣本的分布情況,并且通過DNA和RNA的聯合分析,探索eccDNA與RNA表達之間的關系。如果想短平快的發表5-10分的文章,那么eccDNA表達譜分析顯得再合適不過了。下面這篇文章探索了eccDNA在肌肉組織和血液樣本中的分布情況。小編帶領大家一起解讀這篇高達11分的eccDNA表達譜文章。
小編在這兒也給大家整理了eccDNA表達譜的研究思路,如下圖。
eccDNA優于線性DNA的生物穩定性以及獨特的分子結構特征,為迅速發展的無創活檢道路增添了新的方向,如果有較多的臨床樣本,它非常適合做生物標志物的研究。下面這篇文章是eccDNA在液體活檢方面探索的先驅文章,小編帶大家一起領略其風采。
(3)功能機制
eccDNA作為獨立的DNA分子,如何在細胞中發揮功能和機制是非常重要的問題。目前對eccDNA的功能有一定的研究,前期研究表明eccDNA能夠增強癌基因擴增,近期又有研究證實eccDNA能夠驅動癌基因的基因組重排,可見eccDNA發揮的功能強大,eccDNA的不對稱分布發展模型也逐漸引起了大家的共識——包含eccDNA的癌細胞可能對不斷變化的環境做出快速的反應,包括對癌癥的治療,如放化療。因此未來的研究將需要更好地探索由eccDNA驅動的癌癥是否更容易逃避治療及其潛在的分子機制。相信隨著研究的不斷深入,未來一定會有更多新的功能機制被發現。今天小編在這里給大家匯總一下現有的eccDNA在功能機制方面的研究。下面請跟著編者一起走進eccDNA的新世界,了解這個神奇的分子在癌癥治療方面劃時代的功能。
功能機制一
功能機制二
功能機制三
以上就是我們關于eccDNA的介紹,我們堅信疫情終會過去,科研的腳步從不停留。重量級期刊的文章發表已經為我們新一年的科研指明了方向,游走在線性DNA之外的eccDNA將是生物醫學領域最閃亮的星。新分子,新方向,機遇與挑戰并存,運氣與實力同在,祝愿各位生物醫學的工作者在新的一年能搶占先機,eccDNA將是您科研新年新氣象的不二選擇。
想要云序生物2020年eccDNA線上講座視頻資料可以點擊以下鏈接!
鏈接:http://cloudseq.mikecrm.com/mOePiXY
云序相關產品
環狀DNA測序/eccDNA-seq
RNA-seq
Chip-seq
Cut-tag
外顯子測序
參考文獻
1. Wu Sihan,Turner Kristen M,Nguyen Nam et al. Circular ecDNA promotes accessible chromatin and high oncogene expression.[J] .Nature, 2019, 575: 699-703.
2. Morton Andrew R,Dogan-Artun Nergiz,Faber Zachary J et al. Functional Enhancers Shape Extrachromosomal Oncogene Amplifications.[J] .Cell, 2019, 179: 1330-1341.e13.
3. Paulsen Teressa,Kumar Pankaj,Koseoglu M Murat et al. Discoveries of Extrachromosomal Circles of DNA in Normal and Tumor Cells.[J] .Trends Genet., 2018, 34: 270-278.
4. Møller Henrik Devitt,Mohiyuddin Marghoob,Prada-Luengo Iñigo et al. Circular DNA elements of chromosomal origin are common in healthy human somatic tissue.[J] .Nat Commun, 2018, 9: 1069.
5. Verhaak Roel G W,Bafna Vineet,Mischel Paul S,Extrachromosomal oncogene amplification in tumour pathogenesis and evolution.[J] .Nat. Rev. Cancer, 2019, 19: 283-288.
6. Alt F W,Kellems R E,Bertino J R et al. Selective multiplication of dihydrofolate reductase genes in methotrexate-resistant variants of cultured murine cells. 1978.[J] .Biotechnology, 1992, 24: 397-410.
7. deCarvalho Ana C,Kim Hoon,Poisson Laila M et al. Discordant inheritance of chromosomal and extrachromosomal DNA elements contributes to dynamic disease evolution in glioblastoma.[J] .Nat. Genet., 2018, 50: 708-717.
8. Sin Sarah T K,Jiang Peiyong,Deng Jiaen et al. Identification and characterization of extrachromosomal circular DNA in maternal plasma.[J] .Proc. Natl. Acad. Sci. U.S.A., 2020, 117: 1658-1665.
9. Koche Richard P,Rodriguez-Fos Elias,Helmsauer Konstantin et al. Extrachromosomal circular DNA drives oncogenic genome remodeling in neuroblastoma.[J] .Nat. Genet., 2020, 52: 29-34.
10. Nathanson David A,Gini Beatrice,Mottahedeh Jack et al. Targeted therapy resistance mediated by dynamic regulation of extrachromosomal mutant EGFR DNA.[J] .Science, 2014, 343: 72-6.
11. Turner Kristen M,Deshpande Viraj,Beyter Doruk et al. Extrachromosomal oncogene amplification drives tumour evolution and genetic heterogeneity.[J] .Nature, 2017, 543: 122-125.
電話:021-64878766 郵箱:market@cloud-seq.com.cn
2019年11月,頂尖國際學術期刊《Nature》和《Cell》相繼發表了關于染色體外環狀DNA(extrachromosomal circular DNA,eccDNA)的重要研究,徹底顛覆了人們對癌基因的傳統認知,同時也迅速引爆了整個生物醫學界,一時之間,將人們的目光都吸引到這個科研界的新寵兒身上。

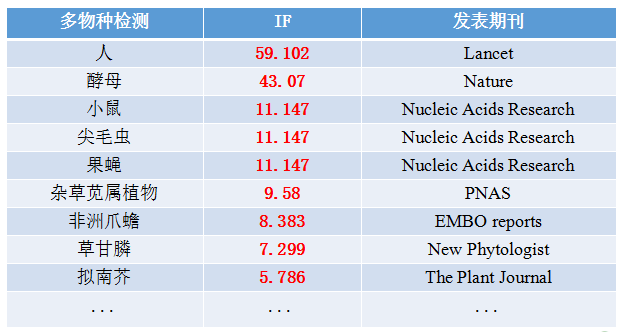
eccDNA 廣泛存在于包括人類的各種真核生物中
其實,這種DNA并不是首次被發現,早在1965年就有關于eccDNA的報道,但當時并沒有引起科學界重視,認為它只是染色體外無意義的垃圾碎片。近年來研究表明,eccDNA往往在腫瘤和衰老過程中富集,以特殊的方式參與腫瘤和衰老的發生發展進程。在大部分人類癌癥細胞中eccDNA廣泛存在,且它的富集通常會促進癌基因的擴增,從而增加了癌基因的可塑性和不穩定性,因此其對腫瘤細胞的進化可能存在重要的意義,這一發現使eccDNA一躍成為科研界的新寵兒。
2. eccDNA的主要特征
(1) 長度特征
目前對eccDNA的大小還沒有定論,eccDNA大部分小于25kb,主要分布在0.1-5KB,但不同的文獻報道中表述略有差別。它們往往是一些特殊的基因區域形成的,可攜帶完整的基因和特殊的調控元件,能獨立完成復制過程,但不攜帶著絲粒和端粒結構。
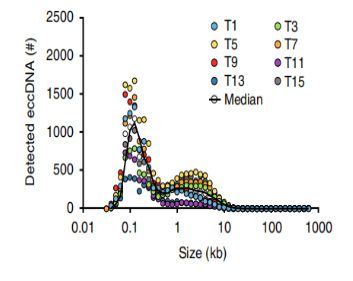
eccDNA的長度分布
(2) 結構特征
早期對eccDNA結構認識比較局限,主要發現它們是環狀DNA分子,并且往往是一些基因擴增的產物,其中也包含著DNA復制起始點,因此可以獨立完成復制作用。2019年,Nature以及Cell文章對eccDNA的結構有了較為深刻的探索分析,發現eccDNA不僅攜帶了完整的基因,還攜帶了基因上游的啟動子和增強子元件。eccDNA的染色質結構更加松散,其中的電鏡照片也清楚的顯示eccDNA為游離在染色體之外的環狀DNA分子。
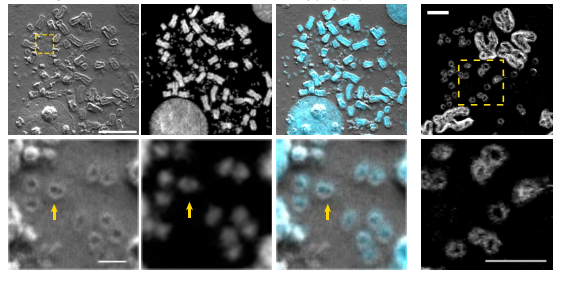
電鏡展示eccDNA的圓環結構
(3) 形成特征
早期的研究發現eccDNA是基因擴增的產物,是基因組不穩定性的一種表現形式。腫瘤基因擴增往往以兩種方式,一種是在染色體上進行基因的擴增,另一種則是形成eccDNA。目前關于腫瘤中eccDNA的形成機制還沒有定論。早期的研究認為短重復序列是介導eccDNA形成的因素,主要通過基因重組機制實現,也有一些模型認為是在DNA復制過程中通過loop切除或在DNA復制暫停的時候復制泡中斷裂的DNA片段連接形成。2018年,Anindya Dutta等在他們的一篇綜述文章中用示意圖展示了各種可能形成eccDNA的分子模型。
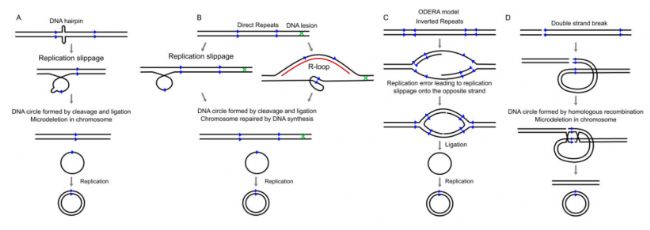
eccDNA可能的形成機制
(4) 表達特征
eccDNA可以攜帶完整的基因,尤其是腫瘤中經常攜帶致癌的驅動基因,不受控制的表達這些基因,最終導致腫瘤的惡性增長。eccDNA是基因擴增的一種形式,對癌基因的表達增高有重要的貢獻。早期的研究聚焦于發現eccDNA的存在,并且是癌基因擴增的重要形式,認為這對癌基因表達的貢獻主要是由于基因拷貝數的增加所致。2019年,Nature和Cell文章表明,eccDNA中染色質高度開放,并且其上存在著增強子序列,這些特征都提高了它的轉錄活性,因此,eccDNA對癌基因的過度表達既有拷貝數增加的因素,更有eccDNA本身高度轉錄活性的貢獻。
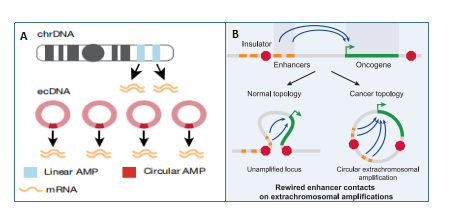
eccDNA通過增加拷貝數和提高轉錄活性增強癌基因擴增
3. eccDNA的常見功能
早期人們一直認為eccDNA的存在是無意義的,直到2014年,Mischel實驗室發現膠質母細胞瘤對EGFR抑制劑的耐藥性是由eccDNA上的EGFRvIII功能獲得性突變的可逆性丟失引起的,人們才重新開始注意ecDNA的功能。檢測結果發現在天然染色體位點上的癌基因擴增相對較少,但是在癌癥中ecDNA的擴增則較為普遍。2017年,Kristen等人通過比較腫瘤基因組和生殖細胞基因組之間的序列,發現在天然染色體位點上的癌基因擴增相對較少,但是在癌癥中eccDNA的擴增則較為普遍。隨后,越來越多的實驗都表明,eccDNA的存在是強大且普遍的,它可以使癌基因在腫瘤細胞中的拷貝數大量增加,而這對于染色體擴增來說是很難實現的。
eccDNA不帶著絲粒元件,因此不能通過有絲分裂的方式均勻分配到分裂后的細胞中。但eccDNA可以通過不對稱分布,在腫瘤細胞中實現定向富集。尤其是攜帶了癌基因的腫瘤細胞,會因為癌基因拷貝數的增高而獲得生長速度的優勢,不對稱分裂過程中攜帶越多的eccDNA,細胞就會獲得越強的生存優勢,因此這種基于不對稱分布狀態的遺傳機制能在快速增殖的細胞中定向富集,因而其擴增使腫瘤能夠快速獲得并維持瘤內遺傳異質性,這也意味著eccDNA在加速腫瘤進化中起著核心作用。
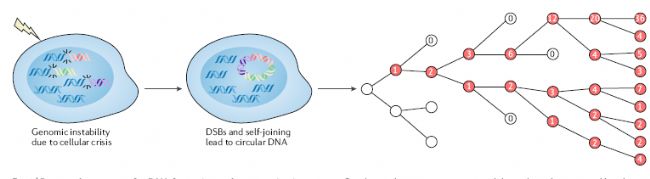
eccDNA通過不對稱分布定向富集
eccDNA作為獨立的DNA分子,在細胞中發揮功能的方式和機制是非常重要的問題。目前對eccDNA的功能有一定的研究,但相信隨著研究的不斷深入,未來一定會有更多新的功能被發現。Anindya Dutta等在他們的綜述文章中系統的匯總了eccDNA的主要功能,如下圖。
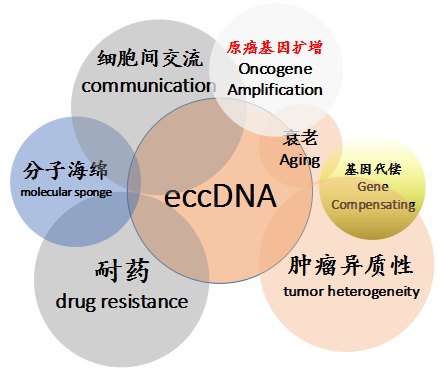
eccDNA常見功能
4. eccDNA的研究思路
所謂兵馬未動,糧草先行!eccDNA的研究也是一場沒有硝煙的戰爭,須得搶占先機,方能知己知彼,百戰不殆。為了各位在這場“戰爭”中取得勝利,云序生物也為大家總結了eccDNA研究的思路。從文章的工作量、難易程度及雜志發表角度看,小編把eccDNA研究思路分為表達譜分析,生物標志物,功能機制研究三大類。那么接下來小編將從這三個角度給大家詳述。

由于eccDNA屬于最新的研究分子,其在眾多物種和疾病中的分布情況都是未知的,這是研究eccDNA首先要解決的問題,也是各位科研工作者最好的一個切入點。不管研究什么內容,首先要做的就是確定好研究物種,疾病模型,樣品類型等基本信息。接下來,通過高通量手段即環狀DNA測序和RNA測序(云序生物提供此服務),確定eccDNA在樣本的分布情況,并且通過DNA和RNA的聯合分析,探索eccDNA與RNA表達之間的關系。如果想短平快的發表5-10分的文章,那么eccDNA表達譜分析顯得再合適不過了。下面這篇文章探索了eccDNA在肌肉組織和血液樣本中的分布情況。小編帶領大家一起解讀這篇高達11分的eccDNA表達譜文章。

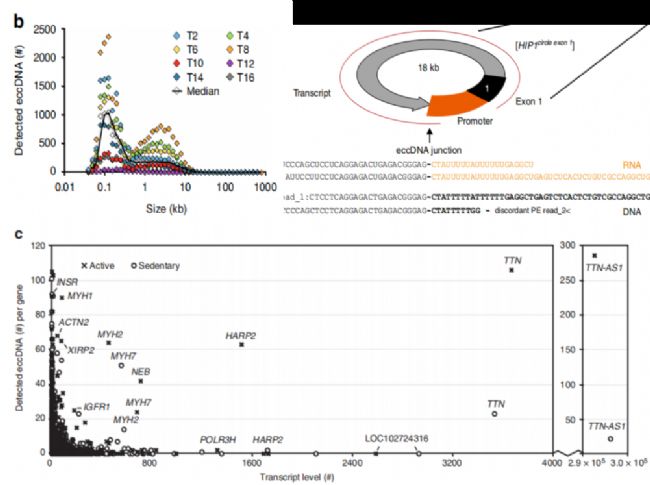
正常組織中eccDNA的分布特征
小編在這兒也給大家整理了eccDNA表達譜的研究思路,如下圖。
eccDNA優于線性DNA的生物穩定性以及獨特的分子結構特征,為迅速發展的無創活檢道路增添了新的方向,如果有較多的臨床樣本,它非常適合做生物標志物的研究。下面這篇文章是eccDNA在液體活檢方面探索的先驅文章,小編帶大家一起領略其風采。

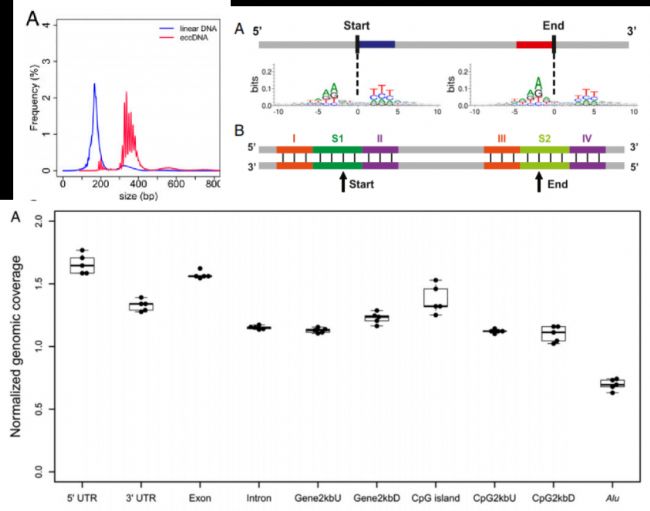
孕婦血漿中eccDNA的特征
(3)功能機制
eccDNA作為獨立的DNA分子,如何在細胞中發揮功能和機制是非常重要的問題。目前對eccDNA的功能有一定的研究,前期研究表明eccDNA能夠增強癌基因擴增,近期又有研究證實eccDNA能夠驅動癌基因的基因組重排,可見eccDNA發揮的功能強大,eccDNA的不對稱分布發展模型也逐漸引起了大家的共識——包含eccDNA的癌細胞可能對不斷變化的環境做出快速的反應,包括對癌癥的治療,如放化療。因此未來的研究將需要更好地探索由eccDNA驅動的癌癥是否更容易逃避治療及其潛在的分子機制。相信隨著研究的不斷深入,未來一定會有更多新的功能機制被發現。今天小編在這里給大家匯總一下現有的eccDNA在功能機制方面的研究。下面請跟著編者一起走進eccDNA的新世界,了解這個神奇的分子在癌癥治療方面劃時代的功能。
功能機制一

功能機制二


功能機制三

以上就是我們關于eccDNA的介紹,我們堅信疫情終會過去,科研的腳步從不停留。重量級期刊的文章發表已經為我們新一年的科研指明了方向,游走在線性DNA之外的eccDNA將是生物醫學領域最閃亮的星。新分子,新方向,機遇與挑戰并存,運氣與實力同在,祝愿各位生物醫學的工作者在新的一年能搶占先機,eccDNA將是您科研新年新氣象的不二選擇。
想要云序生物2020年eccDNA線上講座視頻資料可以點擊以下鏈接!
鏈接:http://cloudseq.mikecrm.com/mOePiXY
云序相關產品
環狀DNA測序/eccDNA-seq
RNA-seq
Chip-seq
Cut-tag
外顯子測序
參考文獻
1. Wu Sihan,Turner Kristen M,Nguyen Nam et al. Circular ecDNA promotes accessible chromatin and high oncogene expression.[J] .Nature, 2019, 575: 699-703.
2. Morton Andrew R,Dogan-Artun Nergiz,Faber Zachary J et al. Functional Enhancers Shape Extrachromosomal Oncogene Amplifications.[J] .Cell, 2019, 179: 1330-1341.e13.
3. Paulsen Teressa,Kumar Pankaj,Koseoglu M Murat et al. Discoveries of Extrachromosomal Circles of DNA in Normal and Tumor Cells.[J] .Trends Genet., 2018, 34: 270-278.
4. Møller Henrik Devitt,Mohiyuddin Marghoob,Prada-Luengo Iñigo et al. Circular DNA elements of chromosomal origin are common in healthy human somatic tissue.[J] .Nat Commun, 2018, 9: 1069.
5. Verhaak Roel G W,Bafna Vineet,Mischel Paul S,Extrachromosomal oncogene amplification in tumour pathogenesis and evolution.[J] .Nat. Rev. Cancer, 2019, 19: 283-288.
6. Alt F W,Kellems R E,Bertino J R et al. Selective multiplication of dihydrofolate reductase genes in methotrexate-resistant variants of cultured murine cells. 1978.[J] .Biotechnology, 1992, 24: 397-410.
7. deCarvalho Ana C,Kim Hoon,Poisson Laila M et al. Discordant inheritance of chromosomal and extrachromosomal DNA elements contributes to dynamic disease evolution in glioblastoma.[J] .Nat. Genet., 2018, 50: 708-717.
8. Sin Sarah T K,Jiang Peiyong,Deng Jiaen et al. Identification and characterization of extrachromosomal circular DNA in maternal plasma.[J] .Proc. Natl. Acad. Sci. U.S.A., 2020, 117: 1658-1665.
9. Koche Richard P,Rodriguez-Fos Elias,Helmsauer Konstantin et al. Extrachromosomal circular DNA drives oncogenic genome remodeling in neuroblastoma.[J] .Nat. Genet., 2020, 52: 29-34.
10. Nathanson David A,Gini Beatrice,Mottahedeh Jack et al. Targeted therapy resistance mediated by dynamic regulation of extrachromosomal mutant EGFR DNA.[J] .Science, 2014, 343: 72-6.
11. Turner Kristen M,Deshpande Viraj,Beyter Doruk et al. Extrachromosomal oncogene amplification drives tumour evolution and genetic heterogeneity.[J] .Nature, 2017, 543: 122-125.
上海云序生物科技有限公司
Shanghai Cloud-seq Biotech Co., Ltd
地址:上海市松江區莘磚公路518號20號樓3樓
網址:http://www.cloud-seq.com.cn
電話:021-64878766 郵箱:market@cloud-seq.com.cn
Copyright(C) 1998-2025 生物器材網 電話:021-64166852;13621656896 E-mail:info@bio-equip.com





